环己基酮(上海有机所Science:酮的动态动力学不对称芳基化和烯基化)
Posted
篇首语:愿君学长松,慎勿作桃李。本文由小常识网(cha138.com)小编为大家整理,主要介绍了环己基酮(上海有机所Science:酮的动态动力学不对称芳基化和烯基化)相关的知识,希望对你有一定的参考价值。
环己基酮(上海有机所Science:酮的动态动力学不对称芳基化和烯基化)
本文来自微信公众号:X-MOLNews
手性醇是一类重要的化合物,广泛存在于药物分子、天然产物、农用化学品以及功能材料中(图1A)。尽管有机金属亲核试剂/氢化物试剂与羰基的不对称加成能以高立体选择性制备含有单个立体中心的醇,但是制备含有两个相邻立体中心醇的方法却很少。通常情况下,利用对映纯α-手性酮的非对映选择性亲核加成可以制备α,β-手性叔醇(图1B),但是这些前体难以制备并且在羰基加成反应或储存期间可能会发生外消旋化。相比之下,利用简单易得外消旋酮和稳定亲核试剂(如有机硼酸盐试剂)的对映汇聚式加成来构建α,β-手性叔醇或许是一个不错的选择(图1C),但是外消旋α-手性酮的动态动力学不对称转化(dynamic kinetic asymmetric transformation,DyKAT)过程要求底物必须快速外消旋化(图1D),而且手性催化剂与底物的一种对映异构体必须快速、高立体选择性进行反应。迄今为止,羰基化合物的动态动力学不对称氢化得到了巨大发展,每年能以超过100吨的规模实现仲醇的不对称合成,但是利用非活化酮的对映汇聚式加成来制备具有相邻立体中心的手性叔醇却尚未见报道,这主要有以下三方面原因:1)非活化底物通过烯醇化进行外消旋的速率缓慢,需要强碱来提高速率,但这限制了官能团耐受性;2)简单酮的亲电性减弱和空间位阻增加会导致加成反应的反应性降低;3)对未活化酮的非对映选择性和对映选择性控制更具挑战性。
近年来,中国科学院上海有机化学研究所施世良研究员(点击查看介绍)课题组长期致力于金属卡宾不对称催化领域的研究。近日,他们利用自主研制的Ni-ANIPE络合物,成功地实现了外消旋非活化酮的动态动力学不对称芳基化和烯基化(图1F),高立体选择性地制备了一系列α,β-手性叔醇,同时还实现了复杂药物分子的后期修饰以及生物活性分子的快速合成。该过程的关键在于供电子NHC-Ni(0)物种可以促进非活化酮的氧化环化以形成η2Ni-酮络合物,再经可逆的β-H消除和重新插入便可实现酮的快速外消旋化。相关成果于发表在Science 上。
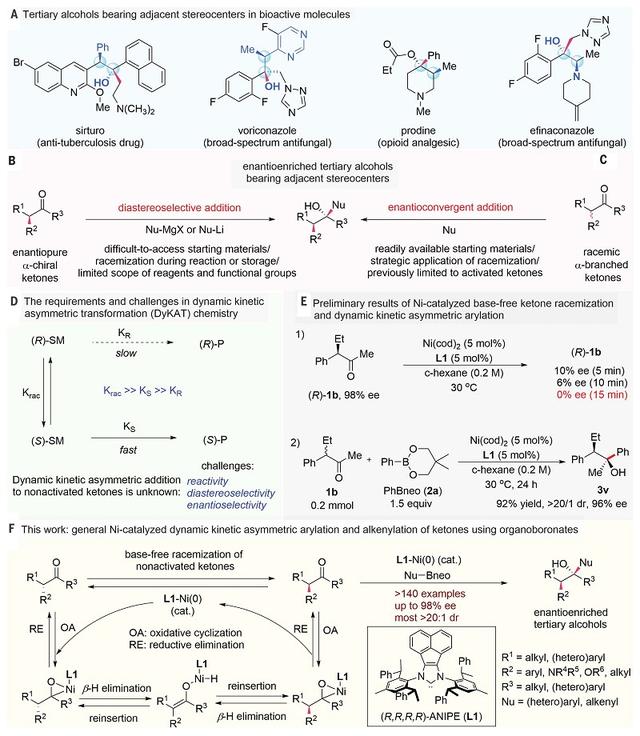
图1. 研究背景及本文设计。图片来源:Science
首先,作者选择外消旋酮1a和苯硼酸新戊二醇酯(Ph-Bneo;2a)为模板底物对反应条件进行优化,并得到最佳条件:即1a(1.0 equiv)和2a(1.5 equiv)在Ni(cod)2(5 mol%)为催化剂、NHC(L1/HCl,5 mol%)为配体、NaOtBu(10 mol%)为碱、环己烷为溶剂的条件下于30℃反应24 h,能以97%的产率、92% ee值和>20:1 dr值得到叔醇3a,在Ni(cod)2(1 mol%)的条件下也能进行克级规模合成并且立体选择性没有降低(图5B)。在最优条件下,作者考察了芳基硼酸酯的底物范围(图2),结果显示一系列富/缺电子基团(如:甲氧基(3c)、甲硅烷基醚(3d)、叔胺(3e)、三氟甲基(3i、3j)、三氟甲氧基(3k)、酯基(3l、3m)、酰胺(3n)、磺酰胺(3p)等)取代的芳基硼酸酯以及杂芳基硼酸酯(如:苯并呋喃(3q)、苯并噻吩(3r)、吲哚(3s)、喹诺酮(3t)、吡啶(3u))均能兼容该反应,以中等至较好的产率和优异的对映选择性、非对映体选择性得到相应的叔醇产物(3a-3u),其中产物3c的绝对构型和相对构型通过X-射线衍射分析证实。其次,作者探究了酮的底物适用性,结果显示α-位带有不同取代基(如:甲基、乙基、大位阻环己基甲基、苄基、肉桂基、异戊二烯基等)的烷基酮(3v-4h)、各种(杂)芳基酮(4i-4r)甚至环状酮(4s-4x)都能高效地转化为所需的叔醇,进一步展现出该方法的通用性。
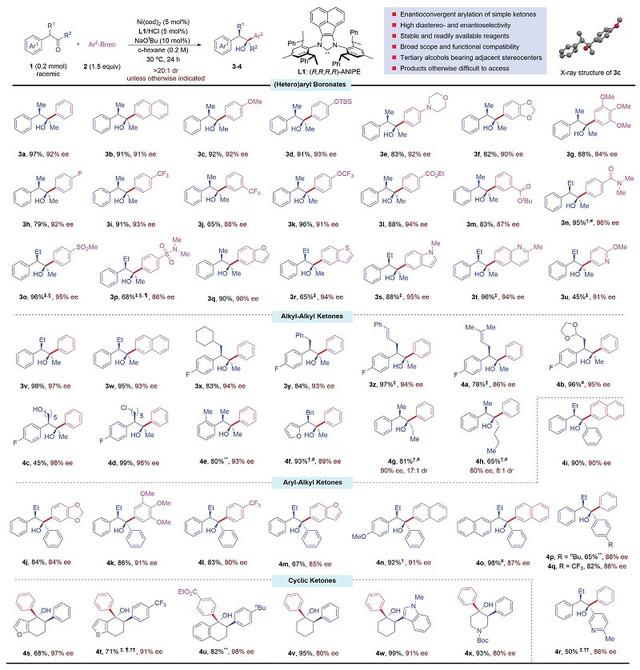
图2. α-芳基酮的对映会聚芳基化底物范围。图片来源:Science
手性氨基醇不仅广泛存在于许多天然产物、药物分子中,而且在不对称合成中还可作为手性助剂、手性配体,因此作者选择外消旋α-苄基(苯基)氨基酮(5a)和Ph-Bneo(2a)为模型底物来合成手性氨基叔醇。对反应条件进行稍加修改后(升温至50 ℃),就能以99%的产率、94% ee值和>20:1 dr值得到手性氨基叔醇6a,并通过X-射线衍射分析证实其绝对构型和相对构型。随后,作者考察了该反应的底物范围(图3),结果显示不同供/吸电子基团取代的芳基硼酸酯(6a-6o)、杂芳基硼酸酯(6p-6s)均能顺利地转化为相应的手性氨基叔醇。含有较长烷基链的二烷基酮(6t-6u)、大位阻的芳基-烷基酮(6v-7a)以及环状α-氨基酮(7b-7f、7q)均能兼容该反应,以中等至较好的产率和优异的对映选择性、非对映体选择性得到所需产物。此外,含有不同取代基的烷基芳基胺(7i-7m)、二烷基胺(7o-7q)甚至N-杂环底物(如:吲哚啉(7c-7f)、二氢喹啉(7g)、四氢苯并氮杂卓(7h)、二氢苯并恶嗪(7n)、吗啉(7p)、哌啶(7q)、吲哚(7r))都能实现这一转化,尽管二烷基胺的反应性和选择性有所降低。值得一提的是,市售的外消旋安息香异丙醚和几种(杂)芳基硼酸酯也能在标准条件下有效地进行偶联,以良好的产率和立体选择性得到相应的β-烷氧基叔醇(9a-9d)。

图3. α-胺基或氧取代酮的对映会聚芳基化底物范围。图片来源:Science
手性对映体纯烯丙醇是有机合成中的重要砌块。虽然目前已经报道了许多不对称方法来合成烯丙基醇,但叔烯丙醇的对映选择性合成却鲜有报道。为此,作者研究了外消旋酮的动态动力学不对称烯基化(图4),发现α-氨基酮(5)与三取代烯基硼酸酯在标准条件下能以95%的产率、95% ee值和>20:1 dr值得到邻位氨基叔烯丙醇11a,还能在较低催化剂负载量的条件下进行克级规模合成。此外,不同基团取代的烷基苯胺(11b-11g)、N-杂环底物(如:二氢喹啉(11i)、二氢苯并恶嗪(11j))甚至α-芳基酮(12a-12h)均能兼容该反应,以中等至较好的产率和立体选择性得到相应产物。需要指出的是,无环/环状底物以及烷基、烯基和芳基取代的烯基硼酸酯都能成功地与α-氨基酮进行偶联并获得所需产物(11k-11s)。
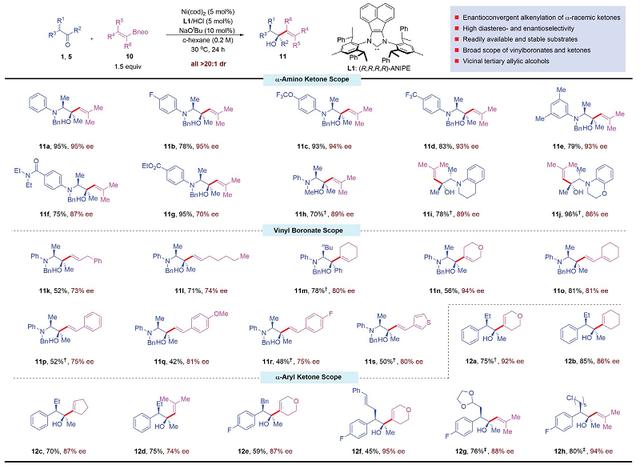
图4. 消旋酮对映会聚烯基化底物范围。图片来源:Science
尽管α,α-二烷基酮的酸性较低,但是大量市售的环状或非环状 α,α-二烷基酮(带有苄基、烯丙基、烷基取代基)则成功地参与了DyKAT芳基化,以高产率和立体选择性得到相应的叔醇(13a-13h,图5A)。值得一提的是,外消旋γ-酮酯可一步法实现对映汇聚式芳基化和随后的内酯化,并以91%的产率、93% ee值、>20:1 dr值得到含有两个相邻立体中心的γ-丁内酯衍生物14(图5C)。随后,作者还利用Watson等人发展的立体保持的镍催化Suzuki-Miyaura偶联方案,成功地将酰化叔醇15转化为复杂分子16,含有两个连续的立体中心,其中一个含有无环全碳季碳中心(图5D)。此外,氨基烯丙醇11a经Pd-催化氢化得到相应的烷基化氨基醇17(图5E),而7o通过Pd-催化的另一个氢化反应得到脱苄基产物18(图5F),它不仅是拟交感神经胺麻黄碱的叔氨基醇异构体,而且还是Pybox配体的合成前体。最后,作者还将DyKAT芳基化策略应用于药物分子(如:布洛芬、萘普生和酮洛芬)的后期修饰,并以高立体选择性得到相应产物(19-21,图5G),尽管21的产率较低,这是因为底物中的两个酮羰基会发生竞争反应。类似地,芳基化产物(13g和13h)经酯化反应分别得到阿片类镇痛药prodine(22)和μ-阿片受体拮抗剂alvimopan的前体23(图5H)。
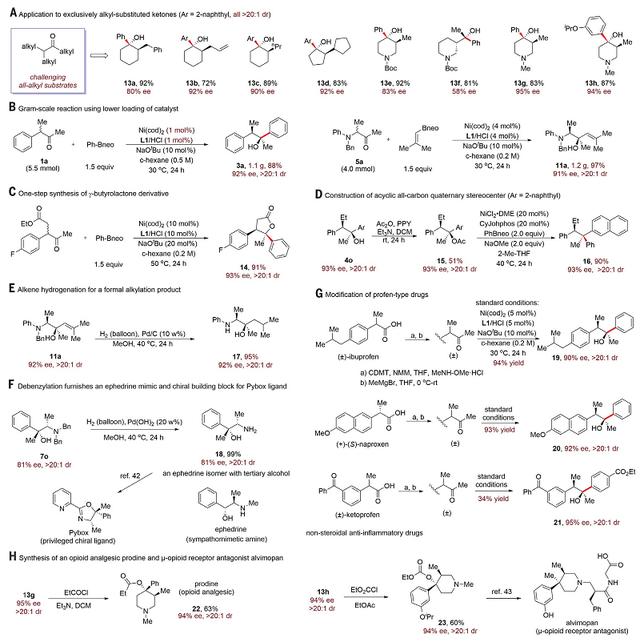
图5. 合成应用。图片来源:Science
为了进一步探究反应机理,作者进行了一系列实验。具体而言:1)(R)-1b、(S)-1b 和(±)-1b分别在标准条件下进行的对照实验表明该过程完全由催化剂控制(图6A),并且(R)-1b是与Ni-L1催化剂立体化学匹配的底物;2)使用L1/HCl的对映异构体[(S,S,S,S)-ANIPE/HCl]进行反应时得到了3v和6a的对映异构体,进一步证实了催化剂控制该过程(图6B);3)酸性较低的α,α-二烷基酮[(R)-1c和(S)-1c] 在无碱条件下也能快速实现外消旋化(图6D);4)对照实验表明外消旋化和C–C键形成过程都在无碱条件下进行(图6E),而且酮外消旋化可能不会通过传统的碱去质子化烯醇化物形成过程进行。在此基础上,作者提出了可能的反应机理(图6F)。首先,手性L1-Ni(0)络合物和匹配的酮底物[(R)-1b]经氧化环化得到氧杂环镍中间体,可通过Ph-Bneo的转金属化开环并形成芳基-烷基镍物种,最后经还原消除便可得到所需产物并再生镍催化剂。需要指出的是,在Ni-NHC络合物的作用下,通过可逆β-H消除和重新插入能有效地将(S)-1b转化为(R)-1b,从而完全消耗酮底物。

图6. 机理研究。图片来源:Science
总结
施世良研究员课题组报道了镍-NHC催化外消旋非活化酮的动态动力学不对称芳基化和烯基化,实现了普适的动态动力学不对称酮加成反应,得到了含两个连续手性中心的复杂叔醇。该反应不仅条件温和、底物范围广、官能团耐受性好,而且为其它挑战性的动态动力学不对称羰基转化提供了新策略。
Dynamic kinetic asymmetric arylation and alkenylation of ketones
Lin-Xin Ruan, Bo Sun, Jia-Ming Liu, Shi-Liang Shi
Science, 2023, 379, 662-670, DOI: 10.1126/science.ade0760
导师介绍
施世良
https://www.x-mol.com/university/faculty/65879
相关参考