片剂脆碎度检测仪(3D打印技术在药物制剂中的应用和挑战)
Posted
篇首语:知识投资收益最大。本文由小常识网(cha138.com)小编为大家整理,主要介绍了片剂脆碎度检测仪(3D打印技术在药物制剂中的应用和挑战)相关的知识,希望对你有一定的参考价值。
片剂脆碎度检测仪(3D打印技术在药物制剂中的应用和挑战)
作者:石靖 ,王增明 ,郑爱萍
3D打印(three-dimensional printing,3DP)是通过建立数字模型层层叠加,逐层打印所需3D产品的技术。3D打印也被称作“快速成型”(rapid forming),“固体自由成型”(solid free forming)和“增材制造”(additive manufacturing)。为响应标准术语的要求,美国机械工程师协会采用“增材制造”作为首选术语,而不是“3D打印”。无论是“增材制造”还是“3D 打印”,关键的区别在于最终产品来自原材料的连续叠加,而不受设备和材料几何形状的影响。3D打印技术具有较高的灵活性,可选用不同性能的材料,如塑料、金属、石膏、聚合物、复合材料甚至活体细胞,经过合理设计,控制打印过程中的工艺参数与系统参数,从而制备出具有各种几何形状和功能的三维产品。近几十年, 3D打印技术发展十分迅速,在航天航空、机械制造、建筑工程及生物医学工程等领域均得到了实际应用。然而,它在制药领域仍处于起步阶段。自20世纪90年代初期以来,很多研究机构一直在进行对3D打印药物递送装置(drug delivery device,DDD)在药物制剂中应用的研究,直到2015年7月,全球首款由3D打印技术研发制备的左乙拉西坦速溶片(商品名:Spritam®)获得美国FDA批准上市,从而使3D打印技术在药物制剂领域获得了极大的关注,也引发了国内外科学家新一轮的研究热潮。本文对近年来应用较多的 3D打印技术及其在药物制剂中的应用进行综述。
1 3D打印技术的分类
3D打印的核心思想最早起源19世纪末的美国,但是直到20世纪80年代中期才有了雏形,1986年美国人Charles Hull应用立体光固化成型技术(SLA)发明了第一台3D打印机。按 照 美 国 材 料 与 试 验 协 会(American Society for Testing and Materials,ASTM)国际标准组织F42增材制造技术委员会(ASTM International Technical Committee F42 on Additive Manufacturing Technologies)的分类,增材制造技术有7种成型工艺,如表1所示。
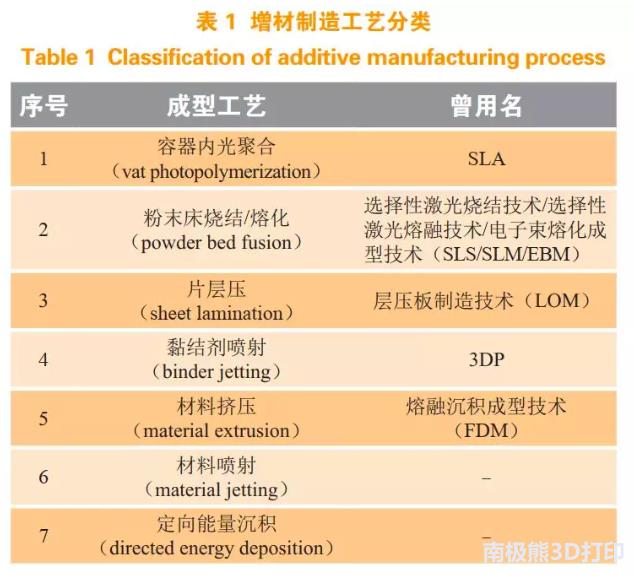
应用在药物制剂领域的主要3D打印技术包括:黏结剂喷射技术、材料挤压技术、SLA。
1.1 黏结剂喷射技术
黏结剂喷射技术是用于制剂生产的主要3D打印技术。典型黏结剂喷射型3D打印机如图1所示。在该示意图中,首先用铺粉辊将粉末均匀地铺在打印机操作台上,打印头在设定好的路径下,以精确的速度将含有黏结剂或者药物的液滴喷射到粉末床上。然后,操作台下降一定距离,再铺洒粉末、滴加液体,如此反复,按照“分层制造、逐层叠加”的原理制备出所需产品。打印过程中未结合的粉末用作打印产品的支撑材料;打印机内的液体制剂可以仅含有黏结剂,粉末床可含有活性药物成分(API)和其他赋形剂;也可以将API 作为溶液或纳米颗粒悬浮液喷射到粉末床上。
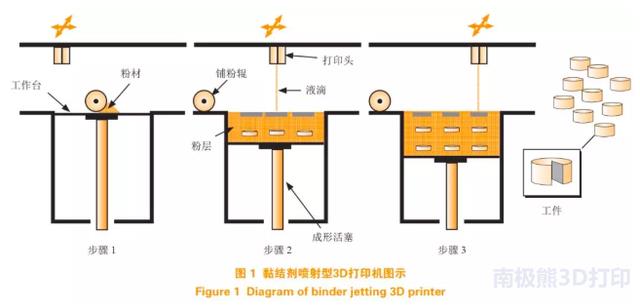
该技术工艺操作中,可调节的参数主要包括:打印液的流速和液滴直径,喷头移动速度,喷嘴与粉末床的距离,粉末铺层厚度,喷涂的次数、角度和位置,滴间距和线间距,以及打印饱和系数等。通过对这些参数的调节,可获得所需制剂的微观结构特性、载药特性等。
黏结剂喷射技术的固化机制与湿法制粒机制相同:在颗粒之间形成基于黏结剂的固体桥或通过溶解和重结晶来形成颗粒。同传统制粒技术一样,使用黏结剂喷射技术时溶剂的选择和粉末的性质会对干燥后API的晶型产生影响。由于与传统制剂生产中使用的制粒技术有诸多相似之处,黏结剂喷射技术有广泛可选的原辅料种类并且在药物制剂中的应用前景广阔。
1.2 材料挤压技术
材料挤压技术是全球范围内最广泛使用的3D打印技术,药物制剂领域对该技术的关注度也不断增长。在打印过程中,材料从机器喷嘴挤出,与需要粉末床的黏结剂喷射技术不同,材料挤压技术可以在任何基板上进行打印。但是,由于缺少粉末床,挤出的物体通常需要较多的支撑材料。各种各样的材料都可以被用于材料挤压技术,包括熔融聚合物、浆料、胶体悬浮液、硅胶和其他半固体材料。
材料挤压技术中最常见的是FDM。FDM是通过把热熔性材料加热到临界状态,使其呈现半流体状态,然后喷头会在软件控制下沿设计好的轨迹运动,将半流动状态的材料挤压出来,材料瞬时凝固,层层打印成所需的产品。与其他挤出系统使用液体或半固体材料进行打印不同的是,FDM系统使用固体聚合物材料,将其驱动到加热的喷头中进行熔融打印。FDM主要工艺参数包括喷嘴直径、喷头温度、填充速度、挤出速度、分层厚度、环境温度、延迟时间等。
相对于黏结剂喷射技术,FDM和其他挤出系统具有更简单的设备和更灵活的产品设计能力,尤其是对于复杂药物制剂的设计。缺点包括打印过程需要加热,需要打印支撑材料和较慢的打印速度,而且通常挤出材料比喷射材料更黏稠,这会增加打印过程中启动和停止打印流体流动所需的时间。尽管材料挤压技术具有局限性,但该技术简单且灵活,已被开始用于药物制剂产品的开发。
1.3 立体光固化成型技术
SLA是最早商业化使用的3D打印技术之一。SLA成型机按英文全称“stereo lithography apparatus”可直译为“立体平板印刷设备”,我国通常称之为立体光固化成型机,它是实现容器内光聚合工艺的一类增材制造装备。SLA工作原理为使用紫外(UV)激光光束通过数控装置控制的扫描器,按设计的扫描路径照射到液态光敏材料表面,使表面特定区域内的一层材料固化后,升降台下降一定距离,固化层上覆盖另一层液态光敏材料,再进行第二层扫描,第二固化层牢固地黏结在前一固化层上,这样一层层叠加而成三维产品。SLA技术需要控制的主要参数是固化层的厚度,其主要取决于光敏材料所暴露的光能量。另外,光敏材料的选择也是至关重要的,应能满足用紫外光照射时的快速固化。
SLA技术已成功应用于组织工程 [19] 和定制外科植入物的原型制作。SLA打印的高精度和高分辨率使其成为制备具有复杂内部结构的药物递送系统的有吸引力的方法 [21]。在药物制剂领域,SLA已经被研究用于制造透皮贴剂、环形片剂和微针等,使用的基础材料为聚乙二醇二丙烯酸酯(PEGDA)。
然而, SLA也有一定的局限性,阻碍了其在药品制造领域的使用。首先,其在药物制剂中的使用受到生物相容性光聚合材料的限制。其次,SLA主要使用单一材料打印,很难用于制造使用多种材料的制剂,例如复杂载药结构制剂。最后,为了能够制造具有更高药物载量的释药系统,原料药必须充分溶解于聚合物中,但现有研究表明,溶解于光聚合物中的药物载量仅有1%~5.9%,而这限制了SLA在高载药释药系统中的应用。但有研究显示,SLA可以实现含有均匀混悬颗粒的聚合物(载药高达 53%)的打印,从而解决载药量低的问题。
2 3D打印技术在药物制剂中的应用
麻省理工学院Sachs等曾于1998年申请了全球首个3D打印技术专利,该专利起初主要被用于汽车部件生产等方面,后来逐渐用于医用假体、组织工程材料、医疗器械与释药系统。2013年以前,每年发表的基于3D打印技术的释药系统相关SCI论文不到20篇;然而,当人们认为3D打印技术用于药物研发尚在起步阶段时,美国FDA已批准了全球首个应用3D打印技术的新药。因此,技术的发展速度往往出人意料。在药物制剂领域,该技术具有空间分布精确、释放精准、药物剂量可控等优势,弥补了传统制药技术的不足,发展前景极为广阔。以下重点对3D打印技术在几种常见剂型,如片剂、植入剂、透皮给药制剂中的应用进行概述。
2.1 片剂
研究人员最早使用黏结剂喷射技术进行3D打印片剂的开发工作,Katstra等使用黏结剂喷射技术,通过调节黏结剂或聚合物浓度,获得了与传统制造工艺硬度和脆碎度相当的片剂;然而,相比于使用传统压片工艺制备的片剂,使用黏结剂喷射3D打印技术制备的片剂通常更加疏松多孔且更易碎。
Aprecia公司在收购麻省理工学院3D药物打印技术后,开发了名为 ZipDose的技术平台,并以3D打印的模式层层制备Spritam®片剂,规格包括250、500、750 和1000 mg。该制剂内部呈多孔状,内表面积大,且制剂表面覆盖有亲水材质,当用一口液体服用时,Spritam® 在口腔中平均崩解时间为11s(范围为2~27s),产生可吞咽的小颗粒。通过实验比较,Spritam® 速溶片在水中的扩散程度要明显大于传统片剂,在少量水中4s即完全崩散。相比于传统药品, Spritam® 最大优势就是能让儿童、老人或有精神障碍等吞咽困难的患者更好地服药,此外,其载药量高(即辅料少)是该技术的另一个重要特点。
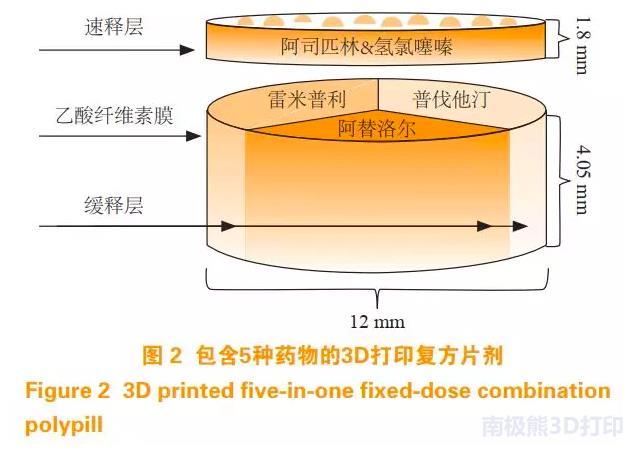
随着3D打印技术的不断发展,其在缓控释制剂制备上的优势越发突出。张惠檄等 [33] 使用挤压式3D打印技术打印了不同形状的阿司匹林双层片,包括速释层包合缓释层的包合打印双层片、速释层在外缓释层在内的同心圆柱体打印片,以及速释层在内缓释层在外的同心圆柱体打印双层片。将3D打印阿司匹林双层片与传统压片机压制的阿司匹林双层片进行比对,各制剂起始均由速释层快速释放,打印双层片的初始释放比传统双层片更快,且最终释放量明显高于压片双层片;而且3D打印机打印的不同形状的片剂具有不同的释放曲线,表明通过程序化设计打印片结构,可以获得所需药物释放行为的片剂。Khaled等使用挤压式3D打印技术制备了含5种药物的复方片剂(见图 2),用于心血管疾病的治疗,该制剂包含 2 种独立的释放机制,其中阿司匹林和氢氯噻嗪为速释部分,普伐他丁、阿替洛尔和雷米普利为缓释部分。制备工艺为将不同原辅料进行搭配,制备成适宜挤出的软材,采用材料挤压式3D打印机按照计算机CAD模型设计的结构,使用特定的喷头挤出不同组分的软材,然后将打印的片剂置于烘箱中干燥固化,即得所需制剂产品。体外释放试验表明,该制剂能够同时满足5种药物的释放,且实验结果表明药物与辅料之间无明显相互作用。该类复方片剂的研究表明,可以将单个药物根据用药需求组合成复杂制剂从而生产个性化药片,解决药物不相容的问题,并提高患者服药的顺应性。
Justyna 等采用 FDM 研制了泼尼松龙缓释片:首先,将聚乙烯醇(PVA)丝材在泼尼松龙甲醇溶液中浸泡 24h,使其充分载药,然后放入烘箱中干燥至恒重,通过计算机软件设计片剂打印参数和调节片剂三维尺寸等参数,即可打印得到不同规格(2 ~ 10 mg)的泼尼松龙缓释片。利用 FDM 制备片剂时,常规的丝材浸泡式方法存在载药量低的问题。Pietrzak 等提出了通过热熔挤出技术(HME)和 FDM 配合使用打印片剂的策略,使其实现高载药量的速释或缓释目标,并使用该技术制备了茶碱控释片。研究中,首先使用 HME 将茶碱和丙烯酸树脂(Eudragit RL)的物理混合物熔融加工成载有茶碱的丝材;利用计算机软件设计拟定尺寸的胶囊形片剂;使用 FDM 3D打印机将载有茶碱的丝材根据设计的图形打印成片剂;3D打印片剂的 SEM 图像显示片剂由 200 μm 的薄层逐层打印而成(见图 3),载药量高达 50%。并且仅通过调节计算机模型设计即可制得不同规格及大小的茶碱控释片(见图 4)。与其他 3D打印材料相比,采用基于 HME 技术制备的丝材作为 FDM 3D 打印机的起始材料具有载药量高、易于存储等诸多优点。
Wang等采用立体光固化成型技术以PEGDA为单体(即合成聚合物的小分子化合物),苯基双 (2,4,6-三甲基苯甲酰基) 氧化磷为光引发剂,分别以 4-氨基水杨酸和对乙酰氨基酚为模型药物,添加聚乙二醇(PEG)300 到打印液中,制备出具有特定释药行为的“甜甜圈”形状的缓释片(见图 5) [23]。其中 4-氨基水杨酸和对乙酰氨基酚的载药量分别为 5.40%和5.69%,整个打印过程中,药物几乎未发生任何降解;而此前的FDM 3D打印试验显示,在打印过程中 4-氨基水杨酸缓释片降解率高达50%。研究证明, SLA 适用于遇热不稳定药物制剂的制备。
此外,不同于传统压片工艺, 3D打印技术可以将药物准确定位于片剂中间或特定部位,除了能精确地控制载药量外,还能起到对药物的保护作用,并防止有毒或高活性药物在生产过程中带来的劳保问题。
2.2 植入剂
植入式给药系统(implantable drug delivery system,IDDS)系由药物与赋形剂经过一定的工艺制备成的一种供腔道、组织或皮下植入用的无菌固体控释制剂。传统制备工艺是先将药物和辅料粉末混合均匀,然后灌注到合适的模具中。该法难以准确控制植入剂的内部结构,因而对其疗效的发挥会产生一定影响。
在发明粉液3D打印技术后,麻省理工学院的研究人员使用3D打印技术研发了可生物降解的植入物,证明了该技术用于药物递送装置的可行性。Wu等使用 3D打印技术,以聚环氧乙烷作为聚合物基质,聚己内酯(PCL)作为控释组分,并用亚甲基蓝和茜素黄染料作为原料的替代物制备各种植入系统。这些研究表明,与传统工艺相比, 3D打印能够通过对微观结构的精确控制,实现对植入剂几何形状、表面积、内部构造以及影响释放动力学的其他属性更好的控制,不仅可以使其在最大程度上与患者的给药部位相吻合,也可以显著减少或消除突释效应,并实现比常规植入剂制造技术更可控的零级释放。

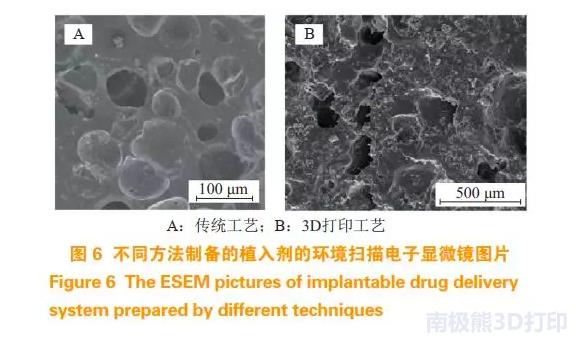
黄卫东比较了传统工艺和 3D 打印技术制备庆大霉素植入式给药制剂的结构,环境扫描电子显微镜(environmental scanning electron microscope,ESEM)结果显示,采用上述2种方法制备的制剂均有明显密布的空隙,水分和体液均可透过空隙并进入制剂内部。3打印制备的植入剂,其整个截面微孔分散均匀,而传统工艺制备的植入剂,其截面微孔较少且大多集聚在一起,大小亦不均(见图 6)。课题组还对上述 2 种制剂的释放行为进行了比较,证实2种方法制备的制剂在体外均呈快速释药。3D打印技术制备的植入剂,其初始释药浓度相对较低,在快速释药后,维持在 8 mg·L-1 以上质量浓度平稳释放,并随时间延长而缓慢降低;传统工艺制备的植入剂,在 2 d 时获得质量浓度为 68 mg · L-1 的快速释药,即药物成分在初始阶段大量释放,后期只能维持约 2 mg · L-1 的质量浓度。Kempin等以奎宁为活性成分,分别采用丙烯酸树脂、聚己内酯、聚乳酸、乙基纤维素作为载体,利用 FDM 制备了活性成分均匀分散的植入剂。在 pH 7.4 磷酸盐缓冲液中进行的溶出研究显示, 4 组溶出曲线差异显著,提示使用该技术制备的植入剂可通过改变材料来获得所需要的释放行为。
2.3 透皮给药制剂
透皮给药系统( transdermal drug delivery system,TDDS)是指在皮肤表面给药,使药物以恒定速率或接近恒定速率通过皮肤,进入体循环并产生全身或局部治疗作用的新剂型,不但可以实现局部定位给药,避免肝脏首过效应,而且可持续控制给药速度。3D打印技术用于透皮给药制剂具有显著优势,尤其是在微针及透皮贴剂领域。
Lu等采用 SLA 3D打印技术,以治疗皮肤癌的达卡巴嗪为模型药物,打印了由25根聚富马酸二羟丙酯微针组成的载药微阵列,以实现化疗药物的透皮给药。其中,微针的尖端和基部直径分别为20和200μm,针头长度仅1 mm,测试结果证明,这些微针完全能承受被插入患者皮肤后可能产生的压力和应力。体外释放试验表明,该载药微针阵列可在长达5周的时间内实现定位释药。这种经皮肤给药的药物传递系统的优势在于患者更加配合、能够控制药物释放等,也包括患者的无痛体验。
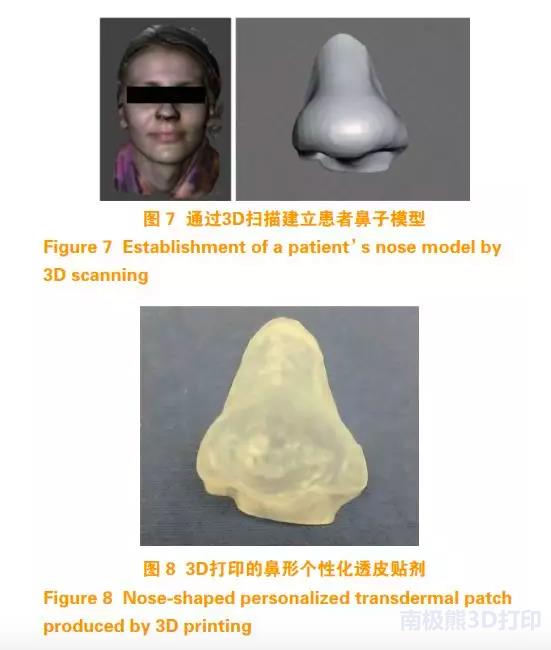
Goyanes等使用3D扫描技术和SLA 3D打印技术配合制备抗痤疮透皮贴剂。使用 3D 扫描技术获得适合于患者鼻子形态的3D模型(见图 7),使用 SLA技术根据3D模型打印鼻形个性化透皮贴剂(见图8)。在 SLA 打印过程中,药物溶解在 PEGDA 和 PEG 的混合物中,混合物通过激光束的作用而固化。实验证明,与 FDM 法相比, SLA 3D打印装置(鼻形)具有较高的分辨率和载药量(质量分数为 1.9%),且没有药物降解。该研究表明, 3D扫描和3D打印的结合可以提供生产个性化载药装置的解决方案,其装置形状和尺寸适用于个体患者的治疗。
3 3D打印技术的优势及意义
虽然目前传统药物生产相对于3D打印制药在批量和成本上更有优势,但是在设计上不够灵活;使用3D打印可以彻底改变药品生产的方式,使其从“一刀切”向个性化、按需制造转变。3D打印与传统制造相比所具有的优势包括:产品设计复杂度、产品个性化和按需制造,这三大优势促进了3D打印药品的开发。
3.1 产品设计复杂度
传统制药技术不具备良好的微观精确控制与空间精准调控能力,与复杂的剂型设计不相匹配,药物3D打印技术于1996年被首次提出,引发了剂型变革的新思路,即剂型开发的数字化设计。使用20世纪技术生产的药品,药物和辅料在产品中的分布几乎完全通过混合或包衣来控制,而剂型开发的数字化设计使剂型发展产生了突破性的变化,使其可以在速释制剂、改良型制剂以及复方制剂的开发中发挥重要作用。
3D打印技术通过控制制剂的外部形状及内部结构可以制备出具有多种结构和释放机制的制剂,为药物递送系统创造了新的机遇。例如, 2015年由FDA批准的3D打印药品Spritam®在不压缩的情况下使粉末黏合,内部的多孔结构使其比传统的速释制剂具有更快的溶出。提高溶出度的策略还包括打印高表面积形状的制剂和通过热熔挤出打印无定形固体分散体,还有研究人员已经使用3D打印技术打印了极低剂量的产品,规格低至3 ng, RSD 为 10%,证明3D打印技术有望用于传统工艺难以实现的极低剂量规格产品的制备。
尽管3D打印可用于速释制剂,但大多数3D打印研究都侧重于改良型制剂。对于寻求更好的控释动力学和药物靶向的药物开发,具有较高设计复杂度的3D打印技术被认为是一个强有力的工具。3D打印可以通过打印材料的选择、模型的设计和工艺参数的调节来控制制剂的外观形状、内部结构、各区域材料组成等因素,从而更好地控制药物释放周期、释放位置及释放速率等。近年来,研究人员正在探索新的产品设计和工艺,以实现新的释药机制。此外,数字化设计对于制造复杂的药械组合产品非常有帮助,研究人员已经使用3D打印技术打印了无线触发胶囊和比一粒米还要小的磁控微载药系统,用于设备控制的口服给药。随着对药械组合产品兴趣的不断增加,研究人员将使用3D打印技术继续开展该领域的研究创新。
3.2 产品个性化
个性化用药是指在充分考虑每个病人的性别、年龄、体质量或遗传因素、生理病理特征等综合情况的基础上制定安全、合理、有效的药物治疗方案。但目前的药物剂量是标准化的,患者往往需要依靠掰开药片获得所需剂量,但通过这种方式无法得到非常精确的剂量,因此标准化剂量的药物无法满足所有患者的需求。而与传统制药相比, 3D打印技术更有助于实现用药个性化,因为数字化设计的调整远比设备的改造更容易,其高度灵活性可以通过修改药片尺寸或填充百分率来实现剂量变化,药剂师可以根据患者的性别、年龄、种族等信息确定最适宜患者的给药剂量和给药形式,然后通过3D打印技术制备出相关制剂,这对于实现患者的个体化用药有重要意义,而且自动化小规模的3D打印运营成本基本可以忽略。简而言之, 3D打印技术在小型化、个性化批次的生产上是经济可行的。
3D打印技术在儿童用药方面也具有独特的优势,可以确保不同成长阶段的儿童能够获得准确的药物剂量,并能实现高活性药物的个体化剂量给药。3D打印技术可以精确控制片剂外观,使用彩色3D打印技术可以打印出特定颜色和形状的制剂,还可以按照儿童喜欢的形状打印出不同的卡通动物药片,从而大大提高临床上儿科用药的患者依从性。此外,个性化给药还包括打印多种药物组合物,将患者需要服用的多种药物组合成单一的日剂量,从而方便服用,这对老年患者来说非常便利,可以防止药物漏服。
3.3 按需制造
3D打印按需制造在时间或资源有限的条件下意义重大,例如在灾区、急诊室、手术室、救护车、重症监护室以及军事行动中。现阶段,3D打印技术在加速新药研发方面具有很大的价值,在新药的临床研究过程中,如果患者对某一剂量的药物没有反应,那么通过3D打印可以迅速制造出不同剂量的药品,这将缩短药物的研发周期。不仅是在新药的临床研究阶段,在药物早期研发阶段, 3D打印技术也能够发挥类似作用。近年来制药行业面临的压力越来越大,在药物开发的早期阶段,开发失败率很高,因此企业希望通过尽可能节约成本的方式识别候选药物分子。潜在的药物必须通过临床前研究,才能进入临床试验阶段,部分研究涉及到测试不同的制剂和剂量以确定其效果。3D打印可以作为替代方案通过提供快速灵活的方法来生产具有不同成分或剂量的小批量药物,从而加速药物的研发。传统的制造工艺往往不支持这种需求,除了剂量不灵活外,还存在药物溶解度和液体制剂稳定性的问题。
此外,与传统制造库存积压不同的是, 3D打印可以在当地完成按需生产,这意味着不存在库存、运输,甚至浪费等问题;同时该技术还能使供应短缺、大型药厂较难生产出的药物制造变得更加容易。
4 3D打印技术目前存在的问题
虽然3D打印技术具有诸多优势,且非常有希望用于个性化剂型的制造,但在广泛用于制药领域之前,仍需要克服一系列技术和监管方面的挑战。
4.1 设备及工艺
制药领域常用的3D打印技术(如黏结剂喷射技术、材料挤出技术)均依赖于打印喷头,根据模型设计层层打印构建有序的产品结构。由于打印喷头在打印单个或多个产品期间需要多次停止和重新启动,因此对于整个生产过程需维持可重现且均一的喷液产生了巨大的挑战。例如,在黏结剂喷射型3D打印过程中,3D打印机的喷嘴堵塞、黏结剂的迁移和渗漏以及粉末进料差异和可能的刮擦都是需要解决的问题。此外,黏结剂喷射型3D打印过程中多余粉末的回收和处理也是生产中必须要考虑的,而且要关注潜在的职业健康危害。同时,与传统制药工艺相比,3D打印药物制剂产业化成本仍然较高。
4.2 产品外观
3D打印的另一个缺陷是产品外观,由于不同聚合物或粉末的彼此堆叠而可能出现产品的表面缺陷,如片剂表面粗糙度、硬度、脆碎度等,而且打印喷头喷出的黏结剂应能形成连续稳定的液滴,但黏结剂的黏度、表面张力以及喷头的精细化程度等因素均会对此产生影响。此外,打印之后的处理过程诸如干燥方法、干燥时间和温度均可能会影响最终产品的外观和质量。这在基于黏结剂喷射技术和材料挤出技术的3D打印中是非常重要的。
4.3 打印材料
到目前为止,与传统的制药工艺相比,可用于3D打印的材料相对有限。对于 FDM,需要使用热塑性聚合物通过从打印喷头挤出来制造产品。对于 SLA,打印材料被限定为光敏聚合物。目前能够满足要求且适用于3D打印制剂生产的材料种类较少,特别是对于个体化给药的特殊剂型,可能需要量身定制的打印材料,而相容性和毒副作用却限制了其他领域材料在药物制剂中的应用。
4.4 监管挑战
3D打印工艺的独特特点,为使用3D打印工艺的药品上市前及上市后的监管,以及质量评价提出了诸多问题。
美国 FDA 已经通过 510(k) 审查并通过了许多3D打印的非植入和植入式医疗器械。2017年12月,美国 FDA 发布了增材制造医疗器械技术考量指南,提供了3D打印产品用于医学应用的初步监管要求,为确保法规的监管方式适合此种独特的创新技术,该指南的建构基于美国 FDA 对100多项使用3D打印的医疗产品进行审查的经验,包含有膝盖置换物、植入物、重建颅骨及 FDA 批准的全球首款3D打印药片。其中提到对于3D打印医疗器械的制造,质量体系控制应该包括物料控制、设计、软件、构建或生产过程、打印后操作(如清洗、灭菌、包装等)、终产品质量控制等所有过程,以确保产品质量,但该指南也指出,目前并不能涵盖所有的监管技术要求。
虽然FDA批准了第一个在 505(b)(2) 途径下提交的3D打印口服剂型,目前尚没有关于3D打印药品方面相关的法规和指导原则。随着3D打印技术在制药领域的应用,相关技术的审评和监管也面临很多未知的问题,比如:3D打印设计中影响药物释放速率和机制的关键因素是什么,如何确定某个 3D几何设计不能达到预期的效果;如何评估3D打印药品的性能,是否可以使用传统的体外测试方法来评价 3D打印药品;如何界定每种3D打印技术的关键工艺参数, 3D打印中间产品的关键特性有哪些;如何进行3D打印制药的质量控制,传统的质量评估方法是否适用,需要什么样的过程控制和验收方法等。
目前FDA药品审评和研究中心药品质量办公室的测试和研究办公室( CDER OTR)正在通过开展研究来解决其中一些问题,与此同时, FDA推出了旨在推进医药创新和现代化先进技术应用的指南,其中也包括了连续制造、 3D 打印技术等等,对有意提交含有新兴技术的申请人在其研究和质控方面提出了一些研究和申报建议。我国的制剂领域的专家,也在推进这一领域的探索和研究。相信科学研究的深入、实践技术的进展以及相关监管法规的完善,必将推动3D打印在制药行业的应用,实现从理论探索进入到现实革命的一个飞跃。
5 结语
3D打印能够按需打印复杂的个性化产品,与传统药物制备工艺相比, 3D打印技术具有极高的可控性和灵活性,非常适合个性化制剂及创新型制剂的制造。由于临床对个性化剂量和特定药物释放行为产品的需求不断增长,3D打印技术在各种药物递送系统的开发及生产中的应用会不断增加,以更好地解决复杂给药方案和特定患者人群的给药问题。近年来,研究人员研发了数十种3D打印创新产品,以提高药物的安全性、有效性和耐受性,该技术的商业可行性已通过FDA于2015 年7月批准的3D打印药片所证实。虽然3D打印技术仍存在诸多技术及监管方面的挑战,但相信通过进一步的发展,目前存在的问题都会得到很好的解决。3D打印将为医药发展带来新的机遇和希望,必将加速个性化、智能化给药时代的到来。
作者:石靖 1,王增明 2,郑爱萍 2
(1.国家药品监督管理局药品审评中心,北京 100038;2.军事医学研究院毒物药物研究所,北京100850)
相关参考
CJY-2C型片剂脆碎硬度测定仪是我司开发的新产品,该产品集测定片剂药物的硬度和脆碎度两种功能于一体。整机结构设计合理,工作性能稳定,操作方便,测试结果精确可靠,主要技术指标均符合《中国药典2015版》标准。广泛...
CJY-2C型片剂脆碎硬度测定仪是我司开发的新产品,该产品集测定片剂药物的硬度和脆碎度两种功能于一体。整机结构设计合理,工作性能稳定,操作方便,测试结果精确可靠,主要技术指标均符合《中国药典2015版》标准。广泛...
01固体口服剂型的优势当前口服固体制剂药物应用非常广泛,是人们比较常见的药品之一。市场占有率多说明固体口服剂型还是有一定的优势的,其稳定性更好、生产成本低、利于携带并且便于服用、患者依从性高。为了更好地...
01固体口服剂型的优势当前口服固体制剂药物应用非常广泛,是人们比较常见的药品之一。市场占有率多说明固体口服剂型还是有一定的优势的,其稳定性更好、生产成本低、利于携带并且便于服用、患者依从性高。为了更好地...
片剂和胶囊剂如何服用(不会吃药简直是玩命不同剂型不同服法需牢记)
作者:上海交通大学医学院附属瑞金医院石浩强有些患者在服用降压药物拜新同(通用名:硝苯地平控释片)后,会发现药物“原模原样”地从粪便中排了出来,大惊失色之下,十分担心药物会没有被吸收而起不到降压的作用。...
片剂和胶囊剂如何服用(不会吃药简直是玩命不同剂型不同服法需牢记)
作者:上海交通大学医学院附属瑞金医院石浩强有些患者在服用降压药物拜新同(通用名:硝苯地平控释片)后,会发现药物“原模原样”地从粪便中排了出来,大惊失色之下,十分担心药物会没有被吸收而起不到降压的作用。...
...了湿热等单元操作,使得对湿热敏感API亦可选择口服固体片剂这种方便的给药形式,DC概念的提出进一步促进了固体口服片剂的发展。目前,DC在新药早期临床制剂开发中应用也较多;由于新药成功概率较低,通过DC这种开发周期...
...了湿热等单元操作,使得对湿热敏感API亦可选择口服固体片剂这种方便的给药形式,DC概念的提出进一步促进了固体口服片剂的发展。目前,DC在新药早期临床制剂开发中应用也较多;由于新药成功概率较低,通过DC这种开发周期...
桌面级3D打印机主要部件图(一张图看懂3D打印的各种技术在铸造业对应哪些应用)
李克强总理形容3D打印用于铸造业带来的变化,说:“刚才我们看的是‘傻大黑粗’,现在已是‘窈窕淑女’了”,那么,3D打印在铸造业到底有哪些神奇作用?科学谷菌说且看3D科学谷一张图。 3DP粘接剂喷射3D打印技术 3...
打印机扫描仪对人体有害吗(皮肤上直接打印3D电子元件 或带来愈合伤口新疗法)
原标题:皮肤上首次直接打印出3D电子元件据物理学家组织网25日报道,在一项开创性的新研究中,美国研究人员使用定制的低成本3D打印机,首次在手上打印出电子产品。借助新技术,战场上的士兵能在身体上打印出临时传感器...