滴定碳酸氢钠和碳酸钠(高考微考点:碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数测定)
Posted
篇首语:山再高,往上攀,总能登顶;路再长,走下去,定能到达。本文由小常识网(cha138.com)小编为大家整理,主要介绍了滴定碳酸氢钠和碳酸钠(高考微考点:碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数测定)相关的知识,希望对你有一定的参考价值。
滴定碳酸氢钠和碳酸钠(高考微考点:碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数测定)
【方法一】分解法测定碳酸钠质量分数
加热混合物固体,碳酸氢钠受热分解,利用加热分解前后的质量变化,由差量法可以得求出碳酸氢钠的含量。
反应:2NaHCO3 = Na2CO3+H2O+CO2↑
【方法二】加酸测定碳酸钠质量分数
题型1:向混合物中加入足量的稀硫酸,测CO2气体的体积或质量(干燥),列方程组计算进而确定Na2CO3的含量。
反应:Na2CO3+H2SO4==Na2SO4+H2O+CO2↑。
2NaHCO3+H2SO4== Na2SO4 +2H2O+2CO2↑
题型2: 混合物样品中加入足量的盐酸,将反应后溶液加热、蒸干、灼烧,得到固体,测量其质量,列方程组计算进而确定Na2CO3的含量。
反应:
Na2CO3 + 2HCl==2NaCl+H2O+CO2↑
NaHCO3+ HCl == NaCl +H2O+CO2↑
【方法三】沉淀法测定碳酸钠质量分数
题型1:将混合物样品配成溶液,向溶液中加入过量的BaCl2溶液,经过滤、洗涤、干燥得BaCO3沉淀,测定质量。进而确定Na2CO3的含量。
反应:Na2CO3+BaCl2===BaCO3↓+2NaCl。
题型2:将混合物样品配成溶液,向溶液中加入过量的Ba(OH)2溶液,经过滤、洗涤、干燥测得BaCO3沉淀的质量。列方程组计算,进而确定Na2CO3的含量。
反应:Na2CO3(少量) + Ba(OH)2 = BaCO3↓+2NaOH
NaHCO3(少量) + Ba(OH)2 = BaCO3↓+ NaOH + H2O
【方法四】利用“双指示剂”(酚酞一甲基橙)测定 Na2CO3 和 NaHCO3
混合物中 Na2CO3 、 NaHCO3 的质量分数
①第一步使用酚酞作指示剂,
滴定原理:Na2CO3十 HCl= NaHCO3 + NaCl ,消耗标准盐酸( V1mL )用于物质转化:Na2CO3→ NaHCO3 ,滴定终点现象是溶液由浅红色变为无色。
②第二步使用甲基橙作指示剂,
滴定原理: NaHCO3 十HCl = NaCl +H20+CO2个,消耗标准盐酸( V2 mL )用于物质转化: NaHCO3 →NaCl ,滴定终点现象是溶液由黄色变为橙色。
【反馈练习】
1.下列试验方案中,不能测定出Na2CO3和NaHCO3的混合物中Na2CO3质量分数的是
A.取ag混合物充分加热,质量减少bg
B.取ag混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到bg固体
C.取ag混合物与足量CaCl2溶液反应,过滤、洗涤、烘干得到bg固体
D.取ag混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,质量增加bg
解析:B.加热后bg固体为氯化钠的质量,设碳酸钠的物质的量为x、碳酸氢钠的物质的量为y, 则106x+84y=a,2x+y = b/58.5, 解方程计算出a、b,然后可计算出混合物中碳酸钠的质量分数;D.ag混合物与足量稀硫酸充分反应,逸出气体主要是二氧化碳和水,所以质量增加bg是此两种气体的质量,故无法求出混合物中碳酸钠的质量分数;
答案选D。
2.下列实验方案中,能测定碳酸钠和碳酸氢钠混合物中碳酸钠质量分数的是( )
A.取a克混合物充分加热,减重b克
B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C.取a克混合物与足量稀盐酸充分反应,逸出气体用碱石灰吸收,增重b克
D.取a克混合物与少量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
【答案】A B
3.实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量。称取1.59 g样品,溶于水配成250.00 mL溶液,取出25.00 mL,该溶液用0.1 mol·L-1盐酸进行滴定,得到如下曲线。以下说法或操作正确的是( )
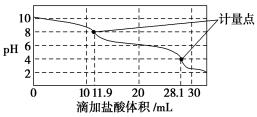
A.第一个计量点之前发生反应的离子方程式:HCO3-+H+=H2O+CO2↑
B.第二个计量点对应溶液中大量存在的阴离子是Cl-、HCO3-
C.此样品中n(NaHCO3)=(28.1-2×11.9)×10-3 mol
D.使用该方法测定Na2CO3和NaOH混合溶液中的NaOH含量,将会得到1个计量点
【答案】C
4.某校课外小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ:甲组同学用称量法,按如图所示的实验流程进行实验:
称量样品 → 加入适量盐酸→ 蒸发结晶 → 称量固体
(1)实验时,蒸发结晶操作中,除了酒精灯、蒸发皿外,要用到的玻璃仪器是___________。
(2)有同学认为“加入适量盐酸”不好操控,应改为“过量盐酸”,便于操作且不影响测定的准确性,该观点____________(填“正确”或“不正确”),其原因是______________.
(3)若实验中测得样品质量为46.4g,固体质量为40.95g,则碳酸钠的质量分数为____________(保留3位有效数字)。
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数将____________(填“偏大”“偏小”或“无影响”)。
方案Ⅱ:乙组同学的主要实验流程如下。

按如图所示装置进行实验:
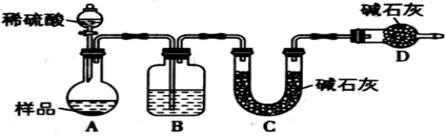
(5)在C装置中装碱石灰来吸收净化后的气体,装置D的作用是_____________________________。
(6)有的同学认为,为了减少实验误差,应在反应前后都通入N2,反应后通入N2的目的是____________。
【答案】(1)玻璃棒 (2)正确 盐酸易挥发,过量的盐酸在加热过程中挥发,不影响结果 (3)45.7%
(4) 偏小 (5)吸收空气中的水蒸气和二氧化碳,以确保U形管中质量增加量的准确
(6)将A、B装置中残留的CO2全部赶入C装置中,减小实验误差
相关参考