溶质和溶剂的概念(数量关系——溶液问题)
Posted
篇首语:白米饭好吃,五谷田难种。本文由小常识网(cha138.com)小编为大家整理,主要介绍了溶质和溶剂的概念(数量关系——溶液问题)相关的知识,希望对你有一定的参考价值。
溶质和溶剂的概念(数量关系——溶液问题)
一、基本知识
1、溶液=溶质+溶剂
2、浓度=溶质÷溶液
3、溶液混合问题:
设两种溶液的质量分别为m1,m2,浓度分别为c1,c2,混合后浓度为c。
那么对于混合问题的解答,有两种方法需要掌握。
(1)方程法
m1c1+m2c2=(m1+m2)c
(2)十字交叉法
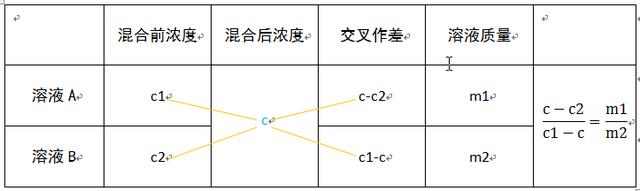
十字交叉法图解
二、趁热打铁
1、使用浓度为60%的硫酸溶液50克和浓度为90%的硫酸溶液若干克,配制浓度为66%的硫酸溶液100克,需要加水的质量是?
A.10克
B.12克
C.15克
D.18克
解析:设需要浓度为90%的硫酸x克。由于混合前后溶质的质量不变,所以有60%×50+90%x=66%×100。解答得x=40,所以混合前溶液共有90克,混合后为100克,所以需要加入10克。答案是A。
2、化学实验中,需要使用现有不同浓度的a、b两种氯化钠溶液配置新的浓度为15%的氯化钠溶液。已知a溶液的浓度是b溶液的5倍,且若将50克a溶液与250克b溶液混合即能完成配置,那么a溶液的浓度是()。
A.45%
B.40%
C.35%
D.30%
解析:利用十字交叉法,如下所示可以解得a溶液浓度为45%。答案为A。
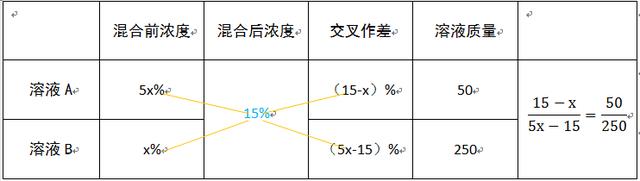
3、有含糖量为7%的糖水600克,要使其含糖量加大到10%,需要再加入多少克糖?
解析:含糖量为7%的糖水600克含有600×93%=558克水;含糖量加大至10%,则糖水共有558÷90%=620克,那么需要加入620-600=20克。
4、例1.甲、乙、丙三种不同浓度、不同规格的酒精溶液,单瓶重量分别为3公斤、7公斤和9公斤,如果将甲乙各一瓶、甲丙各一瓶和乙丙各一瓶分别混合,得到的酒精浓度分别为50%、50%和60%,如果将三种酒精各一瓶混合,得到的酒精中加入多少公斤纯净水后,其浓度为50%?
A.1.2
B.1.3
C.1.6
D.1.9
解析:浓度问题,整个过程溶质不变。如果将甲乙各一瓶、甲丙各一瓶和乙丙各一瓶分别混合,得到的酒精浓度分别为50%、50%和60%”,得到的溶质为:50%×10+50%×12+60%×16=20.6克=2(甲乙丙),甲乙丙各一瓶混合后的溶质为10.3公斤,此时其的浓度为50%,则其的溶液应该为10.3÷50%=20.6公斤,而此时有溶液3+7+9=19公斤,还缺少20.6-19=1.6公斤,故选C。
5、有甲乙丙三种不同浓度的溶液,如果将甲乙按照质量比2:1混合,可以得到浓度为40%的新溶液;如果将甲丙按照质量比1:2混合,可以得到浓度为40%的新溶液;如果将乙丙按照质量比1:1混合,可以得到浓度为27.5%的新溶液。问甲、乙两种溶液按哪种质量比混合,可以得到与丙溶液浓度相同的溶液?
A.1:1
B.2;3
C.3;4
D.4:1
解析:甲乙按照质量比2:1混合和甲丙按照质量比1:2混合都可以得到浓度为40%的溶液,即可写为“(甲甲乙)和(甲丙丙)的浓度相同”即可得到(甲乙)和(丙丙)的浓度相同,故甲乙按照1:1进行混合即可得到与丙相同溶度的溶液,故选A。
6、一个瓶子中装有未知溶液若干,加入一定量的水后浓度变为4%,再次加入与上次相同量的水,溶度变为3%,求,若加入与上次等量的水,溶液的浓度为?
A.2.4%
B.2%
C.1.5%
D.1%
解析:在整个过程中加入的是水,溶质不变。浓度=溶质÷溶液,相当于分子不变,故浓度为4%=12/300,3%=12/400,由此可以看出加入的水为100,故再次加入等量的水,溶质不变依旧为12,溶液为400+100=500,则其的浓度为12÷500=2.4%,故选A。
相关参考