溶解度和溶度积的关系(高中化学沉淀溶解平衡基础)
Posted
篇首语:人生难得几回搏,此时不搏待何时。本文由小常识网(cha138.com)小编为大家整理,主要介绍了溶解度和溶度积的关系(高中化学沉淀溶解平衡基础)相关的知识,希望对你有一定的参考价值。
溶解度和溶度积的关系(高中化学沉淀溶解平衡基础)
01 溶解平衡的建立
在一定条件下,难溶电解质溶于水,当沉淀溶解的速率和沉淀生成的速率相等时,形成溶质的饱和溶液,达到平衡状态,这种平衡称为沉淀溶解平衡。
溶解平衡的特征:溶解平衡同样具有:逆、等、动、定、变等特征。
溶解平衡的表达式:MmAn mMn+(aq)+nAm-(aq);
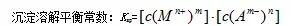
02 影响沉淀溶解平衡的内因
难溶电解质本身的性质。绝对不溶的电解质是没有的。同是难溶电解质,溶解度差别也很大。
影响沉淀溶解平衡的外因:浓度、温度、同离子效应。
03 溶度积规则
在一定温度下,在难溶电解质的饱和溶液中,各离子浓度幂之乘积为一常数,称为溶度积常数,简称溶度积。用符号Ksp表示。对于AmBn型电解质来说,其溶度积的公式是:
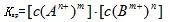
04 沉淀的生成
可通过调节溶液的pH或加入某些沉淀剂实现。
沉淀的溶解:
(1)生成弱电解质。如生成弱酸、弱碱、水或微溶气体使沉淀溶解。
(2)发生氧化还原反应,即利用发生氧化还原反应降低电解质离子浓度的方法使沉淀溶解。
(3)生成难电离的配离子,指利用络合反应降低电解质离子浓度的方法使沉淀溶解。
05 沉淀的转化
沉淀的转化的实质就是沉淀溶解平衡的移动。溶液中的沉淀反应总是向着离子浓度减少的方向进行,简而言之,即溶解度大的生成溶解度小的,溶解度小的生成溶解度更小的。
常见考法
常以选择题的形式考查溶解平衡的特征,溶解平衡的影响因素,溶度积常数与沉淀的转化的关系,这些考题的切入点一般不难,细心计算是第一要务。
误区提醒
1、易溶电解质做溶质时只要是饱和溶液也可存在溶解平衡。如将一块形状不规则的NaCl固体放入NaCl饱和溶液中,一昼夜后观察发现,固体变为规则的立方体,而质量却未发生变化。
2、沉淀的生成、溶解、转化本质上都是沉淀溶解平衡的移动问题。
高中化学沉淀溶解平衡典型例题
题目1、下列有关沉淀溶解平衡的说法中,正确的是( )
A. Ksp(AB2)小于Ksp(CD),说明AB2的溶解度小于CD的溶解度
B. 在氯化银的沉淀溶解平衡体系中加入蒸馏水,氯化银的Ksp增大
C. 在碳酸钙的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动
D. 向氯化银沉淀溶解平衡体系中加人碘化钾固体,氯化银沉淀可转化为碘化银沉淀
答案:D
试题分析:
A.阴阳离子个数比相同的电解质,Ksp越大,溶解度越大,阴阳离子个数比不同的电解质,不能直接根据Ksp的大小判断溶解度的大小,A错误。
B.Ksp只与温度有关,温度不变,Ksp不变,B错误。
C.加入稀盐酸,H+与CO32-反应,平衡向沉淀溶解方向移动,C错误。
D.氯化银溶解度大于碘化银,故氯化银沉淀会转变成更难溶的碘化银沉淀,D正确。
考点:沉淀溶解平衡的相关知识。
题目2、下列有关沉淀溶解平衡的说法正确的是
A. Ksp(AB2)小于Ksp(CD),则AB2的溶解度小于CD的溶解度
B. 在AgCl的沉淀溶解平衡体系中,加入蒸馏水,AgCl的Ksp增大
C. 在AgI的沉淀溶解平衡体系中,加入K2S固体,AgI沉淀可转化为Ag2S沉淀
D. 在CaCO3的沉淀溶解平衡体系中,通入CO2气体,溶解平衡不移动
答案:C
试题分析:
A、AB2和CD的阴阳离子个数比不同,不能通过Ksp大小直接比较溶解度大小,错误;
B、在AgCl的沉淀溶解平衡体系中,加入蒸馏水,温度不变,AgCl的Ksp不变,错误;
C、在AgI的沉淀溶解平衡体系中,加入K2S固体,AgI沉淀可转化为Ag2S沉淀,正确;
D、在CaCO3的沉淀溶解平衡体系中,通入CO2气体,CO2+CO32-+H2O=HCO3-,CO32-的浓度减小,溶解平衡正向移动,错误。
考点:考查沉淀溶解平衡。
相关参考