浓硫酸用什么材质(几种重要的酸和碱)
Posted
篇首语:家资是何物,积帙列梁梠。本文由小常识网(cha138.com)小编为大家整理,主要介绍了浓硫酸用什么材质(几种重要的酸和碱)相关的知识,希望对你有一定的参考价值。
浓硫酸用什么材质(几种重要的酸和碱)

1.硫酸(H2SO4)纯净的硫酸是无色黏稠的油状液体,不易挥发。从工厂生产出来的硫酸常是质 量分数为 98%的浓硫酸,密度为 1.84g/cm3 ,沸点为 338℃。
注 释使用浓硫酸要十分小心,注意防护!用浓硫酸做实验应当穿戴防护服、防 护手套和防护眼镜,避免浓硫酸直接接触身体和衣服。即便是稀硫酸沾到身 上,也要及时洗去,否则,水分蒸发,稀硫酸会变成浓硫酸。 如果不小心将浓硫酸沾在身体和衣服上了,应立即用抹布等物品拭去,迅 速用大量水冲洗。如果沾的浓硫酸量少,可直接用水冲洗。如果硫酸进入眼 中,应立即撑开眼皮冲洗。浓硫酸有吸水性,跟空气接触会吸收空气中的水,因此浓硫酸可作干燥剂,在 保存时应当密封。 浓硫酸还有脱水性,它可以将纸张、木材、衣服、肌肉中的氢、氧元素按水的 组成脱去,使之炭化。

【实验】用玻璃滴管蘸一些浓硫酸在白纸上画画,另用细木条沾一些浓硫酸, 观察现象。 做使用浓硫酸的实验必须有成年人监护,以免发生意外!
用浓硫酸画的画(见图 20-5)很快由无色变为焦黑色,最后纸上沾有浓硫酸 的地方还会被完全烧穿。木条沾有浓硫酸的部分也很快变得同炭一样。在火上烤一下可以加快这一变化。

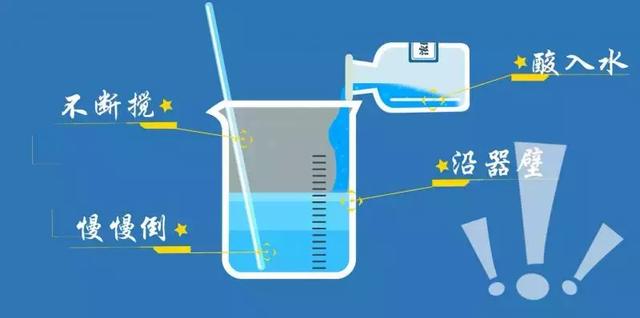
浓硫酸在稀释时,一般应将浓硫酸沿着器壁慢慢注入水中,可用不断搅拌等方 法及时分散浓硫酸。这样在浓硫酸加入水中时,不会因浓硫酸猛烈坠落而溅起水 液,而且一直都是少量的浓硫酸进入多量的水中并沉入水下,在多量水的稀释下, 产生的热量分散到水中,而搅拌又可以使稀释时产生的热量更容易及时分散,因此 可以避免局部水液暴沸。如果将水倒入浓硫酸中稀释,在水刚加入时,只有少量水 进入浓硫酸中,稀释时产生的大量热会使少量的水因暴沸而爆炸,使硫酸飞溅,容 易发生伤害事故。
2.盐酸(HCl)盐酸是氯化氢(HCl)气体的水溶液,在盐酸中,可以检测到 H+和Cl- 。盐酸 和氯化氢气体不是同一种物质,它们在化学性质上有显著的不同,例如盐酸可以使 石蕊试纸变红,干燥的氯化氢气体却不能使石蕊试纸变色。既然盐酸是氯化氢的水 溶液,其中至少含有盐酸和水两种成分,因此盐酸不是纯净物,而是混合物;而氯 化氢是纯净物。 纯净的盐酸是无色液体,工业用浓盐酸常因含有杂质而显黄色。因为盐酸是氯 化氢气体的水溶液,所以盐酸没有 100%的纯品。所谓“纯净的盐酸”,是说其中 没有 HCl和 H2O以外的杂质。 常用浓盐酸的质量分数为 37% ~ 38%,密度约为 1.19g/cm3 。盐酸有挥发性。 浓盐酸在空气中会散发白雾,这是因为浓盐 酸很容易挥发出氯化氢气体,与空气中的水 蒸气结合,形成盐酸小液滴。浓盐酸暴露在 空气中会严重污染空气,不仅有浓烈的刺激 性气味,损害人体健康,还会对周围环境形 成腐蚀性破坏。挥发出的氯化氢气体形成的盐酸会腐蚀电器,同时由于盐酸以及盐酸与电器中金属反应生成的盐溶液都有导电 性,还会造成短路、烧坏电器和触电等事故。所以盐酸应密封保存。 人的胃液里含有盐酸,可以帮助消化。有些胃病患者可能会表现为胃内盐酸不 足,这时医生会给开一些稀盐酸口服。 盐酸也是重要的无机化工原料和化学试剂。盐酸的用途仅次于硫酸,主要用于 医药、食品、电镀、焊接、搪瓷等工业。

3.氢氧化钠(NaOH)氢氧化钠是白色固体,极易溶于水,溶解时会放出大量的热。它的水溶液除有 一般碱溶液的涩味外,还有很明显的滑腻感。 氢氧化钠具有强烈的腐蚀性,所以通常将它叫做烧碱,又叫苛性钠。 氢氧化钠暴露在空气中极易吸水,所以可用作干燥剂。氢氧化钠还很容易与空 气中的二氧化碳反应,因此在保存时要密封。 氢氧化钠会缓慢腐蚀玻璃,因此一般用塑料瓶保存。即便暂时用玻璃试剂瓶存 放氢氧化钠溶液,也不能用玻璃瓶塞,因为玻璃瓶口和玻璃瓶塞受到氢氧化钠腐蚀 后,很容易黏结在一起。 使用氢氧化钠时也一定要十分小心,避免氢氧化钠与身体和衣服接触。用氢氧 化钠做实验应当戴防护眼镜。如果氢氧化钠不小心进入眼中,应撑开眼皮,立即用 水冲洗。

由于氢氧化钠具有强腐蚀性,因此可以用于生产纸浆。 造纸的原料主要是竹木或草类,这些植物材料中除含纤维素外,还含有相当多 的木质素、树胶等非纤维素成分。稀的氢氧化钠溶液不能跟纤维素反应,但能将非 纤维素成分腐蚀溶解,因此用稀的氢氧化钠溶液浸泡造纸原料可以制得以纤维素为 主要成分的纸浆。 氢氧化钠在溶液中很容易与油脂反应,将油脂转化为易溶于水的物质,因此氢 氧化钠具有很强的去油污能力,也常用于工业除油。 氢氧化钠作为化工原料主要用于化学药品、造纸、肥皂、石油、纺织等工业。

4.氢氧化钙氢氧化钙是一种白色粉末状固体,微溶于水,也有腐蚀性,但腐蚀性没有氢氧 化钠强。 氢氧化钙暴露在空气中,容易吸收空气中的二氧化碳,变成碳酸钙,因此在保 存时要密封。 氢氧化钙在水中的溶解度很小,并且比较特殊,随温度升高溶解度反而下降, 20℃时溶解度是 0.165g,100℃时溶解度是 0.077g。 熟石灰广泛用于建筑行业,其主要成分是氢氧化钙。氢氧化钙在化工中可用于 制造氢氧化钠、漂白粉等,在环境保护中可用于大面积消毒,在农业上可用于降低 土壤的酸性以及和硫酸铜溶液混合配制杀菌用的波尔多液等。氢氧化钙还可用于处 理工业酸性废水。
相关参考
1.硫酸(H2SO4)纯净的硫酸是无色黏稠的油状液体,不易挥发。从工厂生产出来的硫酸常是质量分数为98%的浓硫酸,密度为1.84g/cm3,沸点为338℃。注释使用浓硫酸要十分小心,注意防护!用浓硫酸做实验应当穿戴防护服、防护手...
既显弱酸性又显弱碱性的是(101《常见的酸和碱》达标检测(1))
...设计和完成与之有关的实验。熟悉常见的酸—浓盐酸和浓硫酸的物理性质和用途。掌握浓硫酸的稀释方法。【达标检测】()1.某溶液能使酚酞溶液变红,则该溶液会使石蕊溶液A.变红B.变紫C.变蓝D.不变色()2.(10北京)下列溶...
10.1《常见的酸和碱》导学案(3)【学习目标】知道几种常见的碱—氢氧化钠、氢氧化钙等的主要性质和用途。认识碱的腐蚀性及使用时的安全注意事项。认识酸碱溶液通性的原因。【学习过程】一.预习导学1.温故知新:检验...
...起作用而显示不同颜色的物质叫做酸碱指示剂。2、常见的酸碱指示剂有紫色石蕊溶液和无色酚酞溶液。(1)紫色石蕊溶液遇酸溶液(含H+的溶液)变红,遇碱溶液(含OH-的溶液)变蓝,在中性溶液中呈紫色。(2)无色酚酞溶液...
...起作用而显示不同颜色的物质叫做酸碱指示剂。2、常见的酸碱指示剂有紫色石蕊溶液和无色酚酞溶液。(1)紫色石蕊溶液遇酸溶液(含H+的溶液)变红,遇碱溶液(含OH-的溶液)变蓝,在中性溶液中呈紫色。(2)无色酚酞溶液...
氢氧化钠的物理性质和化学性质(中考化学常见的酸和碱知识精讲)
...起作用而显示不同颜色的物质叫做酸碱指示剂。2、常见的酸碱指示剂有紫色石蕊溶液和无色酚酞溶液。(1)紫色石蕊溶液遇酸溶液(含H+的溶液)变红,遇碱溶液(含OH-的溶液)变蓝,在中性溶液中呈紫色。(2)无色酚酞溶液...
浓硫酸,强碱液是化工行业中常见的泵,在输送浓酸和强碱,强腐蚀液体时选用什么材质的泵呢,如选型不当,轻者可造成成本加大、维护工作增多、影响生产,重者可能会导至事故安全,因此如何正确选型成了一个重要的问题...
浓硫酸,强碱液是化工行业中常见的泵,在输送浓酸和强碱,强腐蚀液体时选用什么材质的泵呢,如选型不当,轻者可造成成本加大、维护工作增多、影响生产,重者可能会导至事故安全,因此如何正确选型成了一个重要的问题...
氢氧化钡遇上稀硫酸溶液会发生酸碱中和反应,酸和碱互相交换成分,生成BaSO4沉淀和水分子;两者反应的化学方程式为:Ba(OH)2+H2SO4=BaSO4↓+2H2O。中和反应是什么中和反应实际上指的就是酸和碱相互作用生成盐和水的反应,实...
在大家印象里浓硫酸腐蚀性是很强的,尤其是98%浓度的,听上去就很吓人,看高中化学老师做实验,把白纸扔进浓硫酸里马上就变黑了。可你知道嘛?有一种酸比浓硫酸更恐怖,它就是今天我要讲的氢氟酸。先看看下面这个救援...