氧气的制备(氧气的制法)
Posted
篇首语:一箫一剑平生意,负尽狂名十五年。本文由小常识网(cha138.com)小编为大家整理,主要介绍了氧气的制备(氧气的制法)相关的知识,希望对你有一定的参考价值。
氧气的制备(氧气的制法)
一、工业制氧气
1.原料:空气。
2.原理:利用液态氮的沸点比液态氧的沸点低的原理。先将空气在低温条件下加压变为液态,再将液态空气缓缓升温至-196℃左右,氮气首先达到沸点从液态空气里蒸发出来,剩下的主要就是液态氧了。
3.方法:分离液态空气,其过程可以简单地表示如下:

4.贮存:氧气贮存在蓝色钢瓶中。
【注意】工业上以空气为原料制取氧气,原料来源广泛,所制得的氧气价格较低,量比较大。工业上在制取氧气的过程中,没有新物质生成,属于物理变化。
二、实验室制取氧气
方法一:加热高锰酸钾制取氧气
1、实验药品:高锰酸钾(暗紫色固体)
2、实验原理:高锰酸钾受热时,分解出氧气,同时还有锰酸钾和二氧化锰生成。
3、实验装置:
(1)发生装置
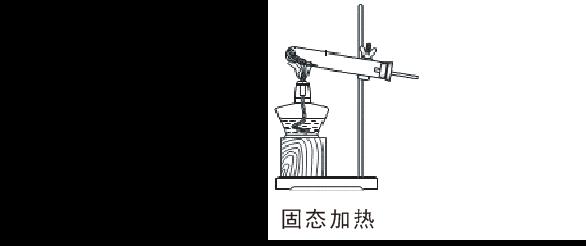
(2)收集装置:
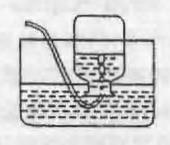
排水法
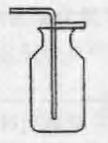
向上排空气法
所以加热高锰酸钾制氧气的实验装置为:
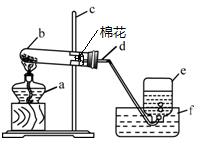
5、实验步骤——"查、装、定、点、收、移、熄"
实验步骤 | 操作方法及注意事项 |
①组装仪器 | 从左到右,自下而上的顺序 |
①检查装置气密性 | 将导管一端浸入水中,用手紧握试管外壁,若水中导管口有气泡冒出,松开手一会儿,导管口形成一段水柱,说明装置不漏气 |
②药品装入试管 | 按固体药品的取用方法,将固体装入试管,平铺在试管底部。试管口部要塞一团棉花,防止加热时,氧气流把氯酸钾粉末吹入导管,使导管堵塞 |
③将试管固定在铁架台上 | 铁夹夹在距离试管口的1/3处; 试管口略向下倾斜,防止冷凝水回流,使试管炸裂 |
④点燃酒精灯加热 | 先预热:先使酒精灯火焰在试管下方来回移动,让试管均匀受热,然后对准试管中药品部位处加热 |
⑤排水法收集氧气 | 集气瓶内装满水,不留气泡,当导管口产生连续气泡时才开始收集;当集气瓶瓶口有大量气泡冒出时停止收集,取出集气瓶,用玻璃片磨砂面盖盖好毛玻璃片,正放在桌面上。 |
⑥收集完毕,移出导管 | 导管不离开水槽,不能熄灭酒精灯,防止水倒吸使试管炸裂。 |
⑦熄灭酒精灯 | 撤离导管后才能熄灭酒精灯,防止水槽中的水倒流入热的试管,使试管炸裂。 |
⑧仪器的拆卸 | 按先右后左,先上后下的顺序。 |
6、检验:将带火星的木条伸入集气瓶内,若木条复燃,证明该气体是氧气。
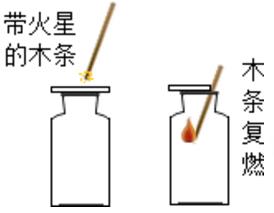
7、验满:用向上排空气法收集到的氧气,验满时,应将带火星的木条放到集气瓶口部,若木条复燃,证明氧气已充满集气瓶。
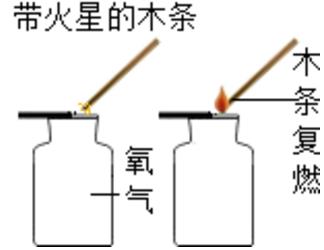
方法二:加热氯酸钾和二氧化锰固体生成氧气
1、实验药品:氯酸钾(白色固体)+二氧化锰(黑色固体)
2、实验原理(文字表达式):

3、实验装置:
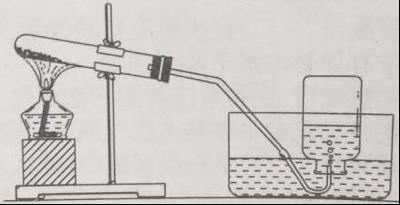
实验步骤:
①查:检查装置气密性。
②装:将氯酸钾与二氧化锰装入干燥的试管,并用带导管的橡皮塞塞紧试管。
③定:将试管固定在铁架台上,注意试管口要略向下倾斜。
④点:点燃酒精灯,试管均匀受热后,就使酒精灯固定在试管底部加热。
⑤收:根据所选的收集装置来确定气体的收集方法。
(注意:当气泡均匀连续冒出时,开始收集气体。当集气瓶口有大量气泡溢出时,证明气体已经收集满。)
⑥移:把导管移出水槽。
⑦熄:熄灭酒精灯。
方法三:分解过氧化氢溶液制氧气
1、实验药品:过氧化氢溶液是无色液体,二氧化锰是黑色粉末。
2、反应原理(文字表达式):
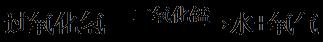
3、实验装置
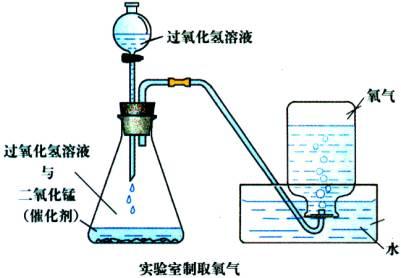
4、实验步骤
(1)在试管中加入5mL5%的过氧化氢溶液,把带火星的木条伸入试管中,观察木条是否复燃。
(2)向上述试管中加入少量二氧化锰,把带火星木条伸入试管,观察现象。
用过氧化氢和二氧化锰制氧气时,如果采用了双孔塞和长颈漏斗,则要求长颈漏斗的下端管口必须_在液面以下_,以防止生成气体从长颈漏斗的下端管口逸出。
3、实验现象:第(1)步中带火星木条不复燃;第(2)步中迅速产生大量气泡,木条复燃
4、实验结论:向过氧化氢溶液中加入二氧化锰后能迅速产生氧气。
三、氧气三种实验室制法的比较(可以自己列一下,加深记忆,尤其是不同点)
过氧化氢制取氧气 | 氯酸钾制取氧气 | 高锰酸钾制取氧气 | ||
发生装置 | ||||
收集装置 | ||||
反应原理 | ||||
试剂状态 | ||||
反应条件 | ||||
相关参考
氧化钙加氧气生成氢氧化钙(化学学习——制取氧气与制取二氧化碳比较)
1,制取比较2,制取思路3,实验室制备气体的探究过程(1)原料药品依据实验目的和化学反应规律确定需要的药品种类及用量。(2)反应原理尊重客观事实和反应规律,写出正确的化学方程式,并且该反应要容易操作和控制,...
一、微生物分类:1.专性需氧菌:必须在有氧气的条件下才能生长,包括大多数细菌、放线菌和真菌。2.微需氧菌:只能在较低的氧含量下正常生长(大气中氧含量通常为20%-21%,而微需氧菌生存环境的氧含量一般为2-10%),如发...
氧气焊焊铁用什么(教焊铁不锈钢铝铜要采用什么焊接方式,好好收藏别弄丢了)
如何焊接低碳钢低碳钢含碳量少,塑性好,可以制备成各种形式的接头和构件。在焊接过程中,不容易产生淬硬组织,产生裂纹的倾向也很小,同时又不容易产生气孔,它是最好焊的材料。采用气焊、手工电弧焊、埋弧自动焊、...
气体加压为什么会变成液体(初中化学:常见气体的性质、制取和用途总结)
一、物理性质补充:1、加压降温后,氧气会变成淡蓝色液体;继续加压降温,会变成淡蓝色雪花状固体。2、固态CO2称为干冰,易升华。二、化学性质三、制法1、反应原理:2、发生装置:选择依据——反应物状态(固体或固液...
...外压缩流程和内压缩流程。全低压外压缩流程生产出低压氧气或氮气,然后经外置的压缩机将产品气体压缩至所需压力供给用户。全低压内压缩流程将
在标准状态下,氧气是一种无色、无味、无臭的活性气体。氧气的存在形态包括压缩氧气和液氧。氧气具有危险危害特性。氧气的典型危害特性包括:1、氧浓度低于23%时,会发生缺氧窒息2、氧浓度较大时(40%),就会发生富氧...
氧气是人类维持生命的三大要素之一,在医院的应用中医院中心供氧系统在临床中有着举足轻重的作用,中心供氧系统是集中解决病人在呼吸方面的氧气供应问题的一种方式。为了确保患者吸入氧气时的舒适度,医护人员通常都...
1、氧气O2标准:2KClO3==(MnO2,加热)2KCl+3O2↑替代:2H2O2==(MnO2)2H2O+O2↑2KMnO4==(加热)K2MnO4+MnO2+O2↑标准制备发生装置:铁架台+酒精灯+试管(塞子和玻璃导管不计)基本无净化(可以干燥,浓硫酸、碱石灰、无水氯化钙均可)收集装置...
氧气的性质图片来源于网络定义:氧气,空气主要组分之一,比空气重,标准状况(0℃和大气压强101325帕)下密度为1.429克/升。无色、无臭、无味。在水中溶解度很小。压强为101kPa时,氧气在约-183摄氏度时变为淡蓝色液体,在...
...即燃烧,呈红色火焰,生成氧化锶(SrO),在加压条件下跟氧气化合生成氧化锶(SrO2)。跟硫、硒、卤素等容易发生化合反应。锶在地壳中的含量约0.04%,丰度居第15位。由于锶极易与空气和水发生化学反应,所以不存在自然态的锶,...