氢氧化钾与二氧化碳反应(2018年中考化学复习方案课时训练八盐化肥)
Posted
篇首语:她其实只是想要个拥抱,可你却总是在讲道理。本文由小常识网(cha138.com)小编为大家整理,主要介绍了氢氧化钾与二氧化碳反应(2018年中考化学复习方案课时训练八盐化肥)相关的知识,希望对你有一定的参考价值。
氢氧化钾与二氧化碳反应(2018年中考化学复习方案课时训练八盐化肥)
课时训练(八) 盐 化肥
1.[2017·株洲]我国制碱工业的先驱——侯德榜先生,1921年留美回国后,潜心研究制碱技术,发明了将制碱与制氨结合起来的联合制碱法(又称侯氏制碱法),为纯碱和氮肥工业技术的发展作出了杰出贡献。下列物质中能与纯碱发生反应的是( )
A.NaOH B.NaHCO3
C.H2SO4 D.K2SO4
2.[2017·盐城]下列属于复合肥的是( )
A.NH4H2PO4 B.NH4HCO3
C.CO(NH2)2 D.K2SO4
3.[2017·无锡]下列有关化肥或农药的叙述错误的是( )
A.硫酸铵属于复合肥料,所含的营养元素是氮和硫
B.氯化铵和磷矿粉从外观即可区分
C.农药施用后,会通过农作物、农产品等发生转移
D.化肥和农药施用不当,会对环境造成污染
4.[2017·鄂州]化肥对提高农作物的产量有重要作用。下列有关化肥的说法不正确的是( )
A.提倡农家肥与化肥综合使用
B.草木灰是一种农家肥,其主要成分中含有钾元素
C.磷肥的主要作用是促进植物茎、叶生长茂盛,叶色浓绿
D.常用作氮肥的化合物有尿素、碳酸氢铵等
5.[2017·庆阳]下列物质间的转化不能一步完成的是( )
A.H2O→H2 B.Mg→MgO
C.Na2CO3→NaOH D.KNO3→NaNO3
6.[2017·济宁]一澄清透明溶液,可能含有H+、Na+、Ba2+、Fe3+、Cl-、OH-、SO42-的一种或几种,为确定溶液中可能存在的离子,进行下面实验:
①经测定,溶液的pH=1
②取部分样品溶液滴加NaOH溶液,有沉淀生成,继续滴加NaOH溶液至不再产生沉淀为止,过滤
③向实验②得到的溶液中滴加Na2CO3溶液,又观察到沉淀生成
分析实验得到的以下结论中,正确的是( )
A.溶液中一定含有H+、Ba2+、Cl-,一定不含有Na+、Fe3+、OH-、SO42-
B.溶液中一定含有H+、Ba2+、Fe3+、Cl-,一定不含有Na+、OH-和SO42-
C.溶液中一定含有H+、Ba2+、Fe3+、Cl-,一定不含有OH-、SO42-,可能含有Na+
D.溶液中一定含有H+、Ba2+、Na+、Fe3+,一定不含有OH-、SO42-,可能含有Cl-
7.[2017·湖州]通过一步化学反应实现如图K8-1所示的X、Y、Z三种物质间的转化,表格中X、Y、Z对应的物质不能实现这种转化的是( )
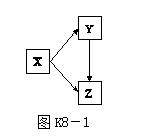
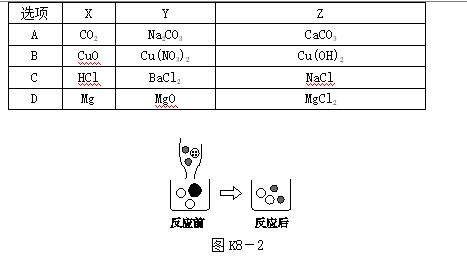
8.[2017·广州]向K2CO3溶液中滴入Ba(OH)2溶液至恰好完全反应。
(1)可以观察到的实验现象是________________。
(2)图K8-2表示该反应前后溶液中存在的主要离子,写出每种图形代表的离子:"

"________;"

"________;"

"________(填离子符号)。
(3)下列物质能与K2CO3溶液反应产生类似上述实验现象的是________(填序号)。
A.Ca(OH)2 B.HCl
C.BaCl2 D.(NH4)2SO4
9.[2017·内江]物质的鉴别、分离和提纯是重要的基本实验操作。
(1)鉴别氢氧化钠和碳酸钠两种溶液,不可选择________(填序号)。
A.氯化钡溶液
B.硝酸钠溶液
C.稀硫酸
(2)除去硝酸钾溶液中混有的少量硫酸钾,可加入适量的硝酸钡溶液,充分反应后过滤即可。写出反应的化学方程式:__________________________________。
10.[2017·郴州]海水中有着丰富的化学资源,人们可以从海水中提取出很多的物质,如:氯化钠、镁等。图K8-3就是利用海水提取氯化钠的大致过程。
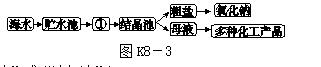
(1)图中①是________(填"蒸发池"或"冷却池")。
(2)析出晶体后的母液是氯化钠的__________(填"饱和溶液"或"不饱和溶液")。
(3)实验室除去粗盐中难溶性杂质的主要实验步骤有:
Ⅰ.溶解;
Ⅱ.________(填操作名称);
Ⅲ.蒸发。
上述三个步骤中,用到的同一种玻璃仪器的名称是________,该玻璃仪器在步骤Ⅱ中的作用是________________。
(4)提取粗盐后的母液中含有较多氯化镁,从母液中提取金属镁的过程大致如下:

该过程中反应Ⅰ的基本反应类型是___________________________________________
写出反应Ⅱ的化学方程式:____________________________________________________。
11.[2017·绍兴]以粗盐(含杂质Na2SO4、MgCl2、CaCl2、泥沙)为原料制备精盐。
(1)加水溶解后,用如图K8-5所示装置除去粗盐中的泥沙,玻璃棒的作用是________。
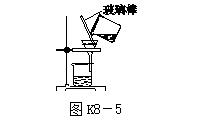
(2)为除去Na2SO4、MgCl2、CaCl2,并得到中性的氯化钠溶液,下列所加试剂和操作:①加过量的Na2CO3溶液、②过滤、③加过量的NaOH溶液、④加适量的稀盐酸、⑤加过量的BaCl2溶液,能达到目的的顺序是________。
A.⑤③②①④
B.③⑤①④②
C.③⑤①②④
(3)用pH试纸检验溶液是否呈中性的操作是______________________________。
12.[2017·连云]港海洋是巨大的资源宝库,从海洋中可以获得很多物质,连云港海水资源丰富。
(1)通过晾晒海水得到的粗盐中含有多种可溶性杂质和不溶性杂质(泥沙等)。实验室中除去粗盐中不溶性杂质获得精盐的步骤是:溶解→过滤→蒸发→计算产率等。
①过滤操作中玻璃棒的末端要轻轻地斜靠在________________一边。蒸发时为防止液滴飞溅,除用玻璃棒搅拌外,还可以采取的操作是______________________________。
②下列操作可能导致精盐产率偏高的是________(填序号)。
a.食盐没有完全溶解即过滤
b.过滤时液面高于滤纸边缘
c.器皿上粘有的精盐没有全部转移到称量纸上
(2)海水中含量最多的氯化物是氯化钠,其次是氯化镁。图K8-6是从海水中获得氯化镁溶液的流程。
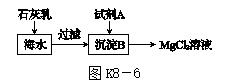
①在海水中加入石灰乳后,发生反应的化学方程式是_____________________________________________________
___________________。
②上述过程中试剂A与沉淀B发生的是中和反应,则试剂A是________(填名称)。
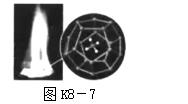
(3)2017年5月18日,在中国南海海域实现可燃冰(CH4·nH2O)试采成功,这将使人类能源格局翻开新篇章。
①可燃冰中,水分子形成一种空间笼状结构,甲烷和少量N2、CO2等分子填入笼内空隙中,无固定的化学计量关系,因此可燃冰属于________(填"纯净物"或"混合物")。
②若某种可燃冰中CH4与H2O的质量比是1∶9,则该可燃冰中n=________。
③可燃冰中甲烷完全燃烧的化学方程式是________________________________________。
[2017·长春]化学试剂厂三个车间排放的废液中分别含有的溶质如下:

按照不同的方式处理,可以得到不同化学产品,从而充分利用资源,变废为宝。
(1)方案一:甲车间废液中加入适量的Na2CO3溶液,可分离回收BaCO3和NaOH,该反应的化学方程式为________________________________________________________________________。
(2)方案二:乙、丙两车间的废液按适当比例混合后,可得到一种溶质为________的中性溶液。
(3)方案三:将三个车间的废液样品混合,过滤。得到无色溶液和白色沉淀。无色溶液中一定含有NaCl,为确定可能含有的溶质,设计下列实验,其中能达到目的的是________。
A.若只加入MgSO4溶液,能观察到明显现象
B.若加入过量的Na2CO3溶液后,再滴加石蕊溶液,都能观察到明显现象
C.若加入过量的中性BaCl2溶液后,再滴加酚酞溶液,都能观察到明显现象
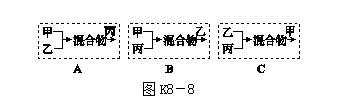
(4)方案四:按照下列方式将三个车间的废液按适当比例混合(假设能反应的物质均恰好完全反应,且中间过程未过滤),最终只生成BaCO3沉淀和NaCl溶液的是________。
14.[2017·烟台]在2017年化学实验操作考试"探究纯碱的性质"中,同学们做了如图K8-9所示的四组实验,并将A、B、C、D四支试管中的废液全部倒入一个干净的大烧杯中。考试结束后,某兴趣小组发现大烧杯底部有沉淀,上层溶液呈红色。为了探究上层溶液的成分,进行了以下实验。
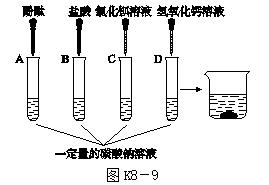
[提出问题] 大烧杯中的上层溶液中除了含有水和酚酞外,还含有哪些离子?(假设难溶物质、水和酚酞均不会解离出离子)
[猜想假设] 小明认为上层溶液中一定含有Na+、CO32-、H+、Cl-、Ba2+、Ca2+、OH-七种离子。你认为上层溶液中含有的离子最多可能有几种,它们分别是________(填离子符号)。
[分析讨论] (1)小红认为上层溶液中一定不含有H+,因为上层溶液呈红色,请你分析上层溶液中不含有H+的另外一个理由:______________________________________。
(2)小李取一定量的上层溶液于试管中,滴加几滴稀盐酸,发现无气泡产生,认为上层溶液中一定不含CO32-。小红认为他的结论不正确,原因是__________________________________________________________________________
______________________________________________________________________。
[设计实验] 为进一步确定上层溶液中是否含有CO32-,请你和小红一起参与下列探究。
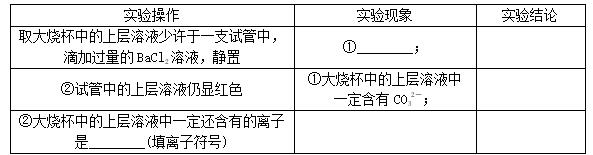
[实验结论] 大烧杯中的上层溶液中一定含有的离子是________________________________(填离子符号)。
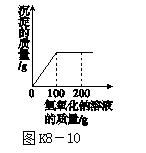
15.[2017·齐齐哈尔]向盛有193.8 g硫酸铜溶液的烧杯中,逐滴加入质量分数为8%的氢氧化钠溶液,反应过程中生成沉淀的质量与所用氢氧化钠溶液的质量关系如图K8-10所示。请计算:
(1)恰好完全反应时,生成沉淀的质量。
(2)恰好完全反应时,溶液中溶质的质量分数。
参考答案
1.C 2.A 3.A 4.C 5.D 6.C 7.B
8.(1)产生白色沉淀
(2)K+ CO32- OH- (3)AC
[解析] (1)向K2CO3溶液中滴入Ba(OH)2溶液时生成碳酸钡沉淀和氢氧化钾,故观察到的现象为产生白色沉淀。(2)K2CO3溶液中有K+和CO32-,二者的个数比为2∶1;Ba(OH)2溶液中有Ba2+和OH-,二者的个数比为1∶2。(3)K2CO3溶液与Ca(OH)2溶液反应生成碳酸钙沉淀和氢氧化钾,与盐酸反应生成氯化钾、二氧化碳气体和水,与BaCl2反应生成碳酸钡沉淀和氯化钾,与(NH4)2SO4不发生反应。
9.(1)B
(2)K2SO4+Ba(NO3)2===2KNO3+BaSO4↓
[解析] (1)氯化钡与氢氧化钠不发生反应,与碳酸钠反应生成碳酸钡白色沉淀,可用氯化钡鉴别氢氧化钠和碳酸钠两种溶液;硝酸钠不与氢氧化钠或碳酸钠发生反应,无法区分这两种溶液;稀硫酸与氢氧化钠溶液反应但无明显现象,与碳酸钠溶液反应时会生成二氧化碳气体,可用稀硫酸鉴别氢氧化钠和碳酸钠两种溶液。(2)硝酸钡与硫酸钾反应生成硫酸钡沉淀和硝酸钾,硫酸钡沉淀可过滤除去,可用适量硝酸钡溶液除去硝酸钾中混有的少量硫酸钾。
10.(1)蒸发池
(2)饱和溶液
(3)过滤 玻璃棒 引流
(4)复分解反应
Mg(OH)2+2HCl===MgCl2+2H2O
11.(1)引流 (2)C
(3)用洁净的玻璃棒蘸取少量溶液,滴在pH试纸上,然后把显示的颜色与标准比色卡对照,读数
12.(1)①三层滤纸 移动酒精灯 ②b
(2)①MgCl2+Ca(OH)2===Mg(OH)2↓+CaCl2
②稀盐酸
(3)①混合物 ②8 ③CH4+2O2eq \\o(=====,\\s\\up7(点燃))CO2+2H2O
13.(1)Ba(OH)2+Na2CO3===BaCO3↓+2NaOH (2)NaCl (3)C (4)B
[解析] (3)将三个车间的废液样品混合,发生的反应有:Ba(OH)2+Na2CO3===BaCO3↓+2NaOH,Na2CO3+2HCl===2NaCl+H2O+CO2↑,过滤,得到无色溶液和白色沉淀,则反应后无色溶液中不含盐酸,无色溶液中除一定含有NaCl外,还含有NaOH或NaOH、Ba(OH)2或NaOH、Na2CO3这三种情况;若只加入MgSO4溶液,由于MgSO4能与NaOH反应产生氢氧化镁沉淀,则这三种情况观察到现象相同,故A不能达到目的;向无色溶液中若加入过量的Na2CO3溶液后,能产生沉淀的为Ba(OH)2,再滴加石蕊溶液,溶液呈蓝色,不能验证有NaOH,故B不能达到目的;向无色溶液中若加入过量的BaCl2溶液后,能产生沉淀,有Na2CO3,再滴加酚酞溶液,溶液呈红色,验证有NaOH,故C能达到目的。(4)甲、乙混合生成了碳酸钡沉淀,在加入稀盐酸时,碳酸钡与稀盐酸反应生成了氯化钡,不会生成碳酸钡沉淀;甲、丙混合生成了氯化钡,在加入碳酸钠时生成了碳酸钡沉淀;乙、丙混合时,碳酸钠与稀盐酸反应生成了氯化钠,再与甲混合时不会生成碳酸钡沉淀。
14.[猜想假设] Na+、Cl-、Ba2+、Ca2+、OH-
[分析讨论] (1)若上层溶液中含H+,则烧杯底部不会有碳酸盐沉淀
(2)上层溶液中含OH-时,滴加少量盐酸,首先发生中和反应,也没有气体产生
[设计实验] 产生白色沉淀 OH-
[实验结论] Na+、Cl-、CO32-、OH-
15.解:(1)设恰好完全反应时,生成氢氧化铜的质量为x,生成硫酸钠的质量为y。
CuSO4+2NaOH===Cu(OH)2↓+Na2SO4
80 98 142
100 g×8% x y
eq \\f(80,98)=eq \\f(100 g×8%,x) x=9.8 g
eq \\f(80,142)=eq \\f(100 g×8%,y) y=14.2 g
(2)恰好完全反应时,溶液中溶质的质量分数为eq \\f(14.2 g,100 g+193.8 g-9.8 g)×100%=5%。
答:(1)恰好完全反应时,生成沉淀的质量为9.8 g;(2)恰好完全反应时,溶液中溶质的质量分数为5%。
相关参考
氢氧化钙和二氧化碳生成什么(河北专版2018年中考化学十四物质的变化与性质认识几种化学反应)
考题训练(十四)__物质的变化与性质__认识几种化学反应|夯实基础|1.[2017·石家庄十八县基础摸底]生活中的下列现象不属于化学变化的是()A.纸张燃烧B.牛奶变酸C.燃放鞭炮D.蜡烛熔化2.[2017·新疆]物质世界充满了变化。下列...
氢氧化钠和氯气反应(中考化学一轮复习——第23讲 氢氧化钠、(氢)氧化钙变质实验)
典题精讲例1下列各组物质相互间不能发生反应的是()A.NaOH、HClB.BaCl2、Na2CO3C.NaCl、Na2SO4D.CuSO4、KOH思路解析:本题考查的是复分解反应发生必须具备的条件,物质相互间不能发生反应就是不具备条件。要使复分解反应发生,必须...
氧化铝和氢氧化钠离子方程式(中考化学一轮复习——第23讲 氢氧化钠、(氢)氧化钙变质实验)
典题精讲例1下列各组物质相互间不能发生反应的是()A.NaOH、HClB.BaCl2、Na2CO3C.NaCl、Na2SO4D.CuSO4、KOH思路解析:本题考查的是复分解反应发生必须具备的条件,物质相互间不能发生反应就是不具备条件。要使复分解反应发生,必须...
氯化镁和熟石灰反应方程式(中考化学专题复习——物质除杂与鉴别的方法)
...酸亚铁溶液反应生成铁和硫酸锌,反应后得不到锌,A错误;氢氧化钠与二氧
氧化镁化学式怎么算出来的(2018年中考化学复习方案课时训练十一化学式化合价)
课时训练(十一)化学式化合价 1.[2017·长沙]2017年5月18日,我国成为世界上第一个连续海上开采可燃冰时间最长的国家,可燃冰的主要成分是CH4,其中碳元素的化合价是()A.-4B.-1C.+1D.+22.[2017·内江]"染色"馒头中添加有...
【注意】CaO放入水中会放出大量的热,这是因为CaO与水反应放热,而不是溶于水放热。【注意】因为Ca(OH)z的溶解度随温度的升高而减少,所以将Ca(OH),饱和溶液转化为不饱和溶液的方法是降低温度。4.饱和溶液、不饱和溶液与浓...
氧化铁与一氧化碳反应(中考化学复习173卷—一氧化碳还原氧化铁)
氢氧化钠不溶于什么物质(2021年中考化学二轮复习第3讲-溶液的形成,溶解度)
...热现象。如硝酸铵溶解时会吸热,表现为溶液的温度降低;氢氧化钠溶解时会放热,表现为溶液的温度升高。【注意】氧化钙遇水也会放出大量的热,但这一
...+酸=盐+水(4)碱+某些盐=另一种盐+另一种碱1、氢氧化钠跟二氧化碳反应:2NaOH+CO2=Na2CO3+H2O2、氢氧化钠跟二氧化硫反应:2NaOH+SO2=Na2SO3+H2O3、氢氧化钠跟三氧
氧化钠与二氧化碳反应(中考名师总结:初中化学常见物质性质,考试得分必备)
中考名师总结:初中化学常见物质性质,考试得分必备!一、固体的颜色1、红色固体:铜,氧化铁2、绿色固体:碱式碳酸铜3、蓝色固体:氢氧化铜,硫酸铜晶体4、紫黑色固体:高锰酸钾5、淡黄色固体:硫磺6、无色固体:冰,...